پروفایل بیان ژن: تفاوت میان نسخهها
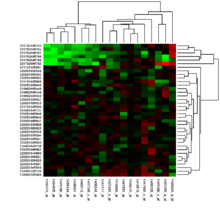
صفحهای تازه حاوی «پرونده:Heatmap.png|جایگزین=نقشهی گرمایی از مقادیر بیان ژن نشان میدهد چگونه شر...» ایجاد کرد |
(بدون تفاوت)
|
نسخهٔ ۲۰ اوت ۲۰۱۷، ساعت ۲۱:۵۱
در حوزهی زیست مولکولی، اندازهگیری پروفایل بیان ژن معیاری از فعالیت هزاران ژن به صورت یکجا، برای ایجاد یک تصویر عمومی از کارکرد سلول است. این پروفایل میتواند برای مثال بین سلولهای فعال جدا از هم تمایز ایجاد کند، یا مشخص کند یک سلول چگونه به یک درمان واکنش نشان میدهد. بسیاری از آزمایشهای در این سطح، کل ژنوم را به صورت همزمان، برای هر ژن، در یک سلول خاص اندازهگیری میکنند.
تعداد زیادی تکنولوژی ترانسکریپتوم برای تولید دادهی مورد نیاز برای آنالیز میتواند مورد استفاده واقع شود. ریزآرایهی دیاِناِی[۱] فعالیت نسبی یکسری ژن هدف را اندازه میگیرد. تکنولوژیهای مبتنی بر دنباله، مانند توالییابی آرانای علاوه بر سطح بیان ژنها، اطلاعاتی از دنبالهی آنها را نیز فراهم میکنند.
مقدمه
بدست آوردن بیان ژن، مرحلهی منطقی پس از توالییابی ژنوم است: دنبالهی ژنوم به ما این اطلاعات را میدهد که سلول چه فعالیتهایی انجام میدهد، در حالی که پروفایل بیان ژن مشخص میکند دقیقا در آن لحظه چه کارهایی انجام میشود. ژنها شامل دستورهایی هستند که آراِناِیهای پیامرسان (mRNA) را میسازند، اما در هر لحظه هر سلول فقط بخشی از ژنهایی که دارد را به mRNA تبدیل میکند. چنانچه ژنی، در حال تولید mRNA باشد، آن ژن "روشن" و در غیر این صورت "خاموش" در نظر گرفته میشود. معیارهای زیادی مشخص میکنند که یک ژن روشن یا خاموش باشد، از جملهی آنها میتوان به زمان، محیطی که در آن قرار دارد و سیگنالهای شیمیایی که از سلولهای دیگر دریافت میکند اشاره کرد.
بررسی پروفایل بیان ژن، معمولا اندازهی نسبی بیان mRNA ها را در دو یا چند شرایط آزمایشگاهی بدست میآورد. به این دلیل که تغییرهای سطح بیان یک دنبالهی مشخص از mRNA، تغییرهایی در پروتئین حاصل از آن ژن را نشان میدهد، که میتوان نمایندهی یک شرایط آسیبدیده یا پاسخ همایستایی باشد. برای مثال سطح بیان بالای mRNA ای که الکل dehydrogenase را کد میکند نشاندهندهی این است که سلولها یا بافت مورد بررسی، در حال پاسخگویی به افزایش سطح اتانول در محیط است.[۲][۳][۴]
مقایسه با پروتئومیک
ژنوم انسان شامل حدود 5000 ژن میباشد که در حدود 1،000،000 پروتئین متفاوت را تولید میکنند. این بهخاطر پیرایش جایگزین است و همینطور به خاطر اینکه سلولها تغییرهایی را پس از اینکه بار اول پروتئین را ایجاد کردند، در پروسهی پیرایش پسارونویسی ایجاد میکنند، و در نتیجه، هر ژن میتواند پایهای برای تولید نسخههای متفاوت پروتئین باشد. با یک آزمایش mass spectrometry میتوان حدود 2000 پروتئین یا 0.2% از کل پروتئینها را شناسایی کرد.[۵] اطلاعاتی که از خود پروتئینها (پروتئومیک) بدست میآید از اطلاعاتی که از RNA های پیامرسان استخراج میشود دقیقتر است.[۶]
کاربرد در تولید و آزمون فرضیه
در بعضی مواقع، یک دانشمند فرضیهای در ذهن دارد و در مورد اتفاقهایی که ممکن است بیفتد ایدههایی دارد، و با انجام آزمایشهای پروفایل بیان ژن سعی دارد این فرضیه را رد کند. در حقیقت دانشمند پیشبینیای در مورد سطح بیان سلولی میکند که ممکن است اشتباه باشد.
معمولا پروفایل بیان ژن زمانی بدست آورده میشود که اطلاعات کاملی در مورد تعامل ژنها با شرایط آزمایشگاهی در مورد یک فرضیهی در حین آزمون نداریم. بدون فرضیه، چیزی برای انکار کردن یا اثبات کردن وجود ندارد، اما پروفایل بیان میتواند برای شناسایی فرضهای کاندید برای آزمایشهای آینده کمککننده باشد. بسیاری از آزمایشهای پروفایل بیان ژن ابتدایی و امروزی، به صورت "اکتشاف کلاس" شناسایی میشوند که به فرمی است که در ادامه توضیح داده میشود.[۷] روش معروف برای اکتشاف کلاس شامل گروهبندی کردن ژنها یا نمونههای مشابه با استفاده از خوشهبندی کی_میانگین یا سلسلهمراتبی میباشد. مستقل از روش خوشهبندیای که مورد استفاده قرار میگیرد، نیاز است کاربر معیار فاصلهی مناسبی (فاصله یا شباهت) بین دادهها برگزیند.[۸] تصویر بالا خروجی خوشهی دوبعدی را نشان میدهد، به طوری که نمونههای مشابه (سطرها) و پروب ژنهای مشابه (ستون) به گونهای مرتب شدهاند که نزدیک هم قرار دارند. سادهترین شکل اکتشاف کلاس، لیست کردن همهی ژنهایی است که بین دو شرایط آزمایشگاهی بیشتر از یک حدی تغییر کردهاند.
پیشبینی کلاس از اکتشاف کلاس بسیار سختتر است، اما این امکان را به افراد میدهد که به سوالهای مهمی که مستقیما بالینی هستند پاسخ دهد. برای نمونه با دادن این پروفایل امکان این که بیمار به یک داروی خاص پاسخ دهد چقدر است؟ پاسخ به این سوال نیاز به تعداد زیادی نمونه از پروفایل دارد که به دارو پاسخ دادهاند و تعدادی که پاسخ ندادهاند.
اعتبارسنجی اندازهگیریهای با حجم بالا
هر دو تکنولوژی ریزآرایهی دیانای و واکنش زنجیرهای پلیمراز بلادرنگ (qPCR) ، از جفتبازهایِ دنبالهی مکمل نوکلئیک اسید استفاده میکنند، و هر دو در بدست آوردن پروفایل بیان ژن، معمولا در یک روش سریالی استفاده میشوند. در حالی که تکنولوژی حجم بالای ریزآرایهی دیاِناِی دقت qPCR را ندارد، اندازهگیری بیان ژن چندین ژن با استفاده از qPCR و اندازه گیری کل ژنوم با استفاده از ریزآرایهی دیانای تقریبا زمان یکسانی میبرد. بنابراین منطقی است که ابتدا آزمایشهای تحلیل ریزآرایهی دیانایِ شبه کمّیای برای شناسایی ژنهای کاندید انجام شود، سپس qPCR روی تعدادی از ژنهای جالب بدست آمده در مرحلهی قبل انجام شود.
تفسیر ژن
در حالی که ممکن است آمار شناسایی کند کدام محصول از ژن تحت شرایط آزمایشگاهی تغییر میکند، تفسیر و درک ابعاد زیستی بیان ژن بستگی به این دارد که بدانیم هر پروتئین از کدام ژن بدست آمده است و چه عملکردهایی دارد. تفسیر ژن اطلاعات عملکردی و دیگر اطلاعاتی مانند مکان ژن در کروموزوم را فراهم میکند. بعضی از تفاسیر عملکردی نسبت به سایر تفاسیر قابل اعتمادتر هستند. پایگاه دادهی تفسیر ژن به صورت مرتبط تغییر میکند و پایگاه دادههای متفاوت به یک پروتئین یکسان با نامهای متفاوتی اشاره میکنند، و نشاندهندهی این است که درک عملکرد پروتئین مدام در حال تغییر است.[۹][۱۰]
دستهبندی ژنهای تنظیمشده
پس از شناسایی مجموعهی ژنهای تنظیمشده، مرحلهی بعدی بدست آوردن پروفایل بیان ژن است که در برگیرندهی جستجوی الگویی بین مجموعهی تنظیم شده است. سوالی که مطرح میشود این است که آیا پروتئینهایی که از این ژنها بدست میاد عملکردهای مشابهی دارند؟ آیا از نظر شیمیایی مشابه هستند؟ آیا در موقعیت مشابهی از سلول قرار دارند؟ تحلیل هستیشناسی ژن روش استانداردی برای تعریف این روابط میباشد. هستیشناسی ژنها با دستهبندی بسیار وسیعی شروع میشود، برای مثال "فرآیند سوختوساز" و آنها را به دستههای کوچکتر تقسیم میکند.
ژنها در کنار عملکرد زیستی، ویژگیهای شیمیایی، و موقعیت سلولی، ویژگیهای دیگری هم دارند. میتوان مجموعهای از ژنها را برحسب میزان نزدیکیشان به ژنهای دیگر با هم ترکیب کرد و ارتباطشان با یک بیماری، داروها یا سمها را بدست آورد.
یافتن الگویی بین ژنهای تنظیمشده
ژنهای تنظیمی با توجه به اینکه چه کاری انجام میدهند و چه هستند دستهبندی میشوند، و ممکن است ارتباطهای مهمی بین ژنها بدست آورده شود. برای نمونه، ممکن است شواهدی صورت گیرد که یک ژن خاص، پروتئینی میسازد که آن یک آنزیم را ایجاد میکند و آنزیم تولید شده، پروتئین دیگری را فعال میکند که باعث میشود ژن دوم دیگری در لیست روشن شود. این ژن دوم ذکر شده ممکن است یک سازه رونویسی باشد که ژن دیگری از لیست ما را تنظیم میکند. مشاهدهی این ارتباطها، ما را مشکوک میکند که این لیست، ارتباطهای فراتر از شانس با یکدیگر دارند و همهی آنها به خاطر یک فرایند زیستی پایه در لیست ما قرار گرفتهاند. از طرفی اگر چند ژن به صورت رندم انتخاب کنیم، میتوان تعدادی ژن مرتبط با آنها پیدا کرد. در این موارد، به پردازشهای آماری دقیقی نیاز داریم تا مشخص شود آیا نتیجهی زیستی بدست آمده معنادار هست یا نه. در این شرایط تحلیل مجموعهی ژنها مورد نیاز است.
رابطهی علل و معلول
ابتدائا تحلیلهای آماری ساده مشخص میکند آیا ارتباط بین ژنهای درون لیست بیشتر از مقداری است که میتواند شانسی باشد. این آمار حتی در صورتی که بیش از حد سادهسازی شده باشد، میتواند جالب باشد. یک مثال را بررسی میکنیم، فرض کنیم در یک آزمایش 10000 ژن داریم، فقط 50 درصد آنها نقشی در ساختن کلسترول بازی میکنند. آزمایش 200 ژن تنظیمی را تشخیص میدهد. در بین این 200 ژن 40 عدد در بین لیست ژنهای تاثیر گذار در کلسترول هستند. با توجه به تعداد ژنهای کلسترول در کل (0.5%)، انتظار میرود به ازای هر 200 ژن، یکی از آنها جزو ژنهای تاثیرگذار در کلسترول باشد، که برابر است با 0.005 برابر 200. این پیشبینیِ مورد انتظار است و ممکن است کسی بیشتر از یک ژن مشاهده کند. سوال این است که چه زمانی ما میتوانیم به صورت شانسی به جای 1 ژن 40 ژن مشاهده کنیم.
با توجه به توزیع فوق هندسی، انتظار میرود باید حدود 57^10 بار لیست 200 تایی ژن به صورت تصادفی انتخاب شود تا بتوان یک لیست شامل 39 یا بیشتر، ژن مشترک با لیست تاثیرگذار در کلسترول در آن پیدا کرد. چنانچه ممکن است از جنبهای، مشاهدهی تصادفی این مورد بسیار کوچک به نظر آید، ممکن است کسی نتیجه بگیرد که لیست ژنهای تنظیمی، بسیار غنی از ژنهای مربوط به کلسترول هستند.[۱۱]
ممکن است فرض شود اِعمال شرایط خاص در آزمایش، باعث تنظیم کلسترول شده است، زیرا نحوهی درمان به نظر گونهایست که ژنهای مربوط به کلسترول را تنظیم میکند. در حالی که ممکن است این فرضیه درست به نظر برسد، دلایلی وجود دارد که نتیجهگیری بر اساس غنی بودن به تنهایی، نتیجهی غیرقابلتوجیهی را میدهد.
نتیجهگیری
بدستآوردن پروفایل بیان ژن، اطلاعات جدیدی در مورد اینکه ژنها در شرایط متفاوت چه کارهایی میکنند به ما میدهد.[۱۲] بهطور کلی، تکنولوژی ریزآرایه، پروفایل بیان ژن قابل اطمینانی فراهم میکند. با استفاده از این اطلاعات میتوان فرضیههای جدیدی در مورد واقعیتهای زیستی یا آزمایشی بدست آورد. اگرچه اندازه و پیچیدگی این آزمایشها معمولا منجر به انواع متنوعی از تفاسیر میتواند بشود. در بسیاری از موارد، نتیجهی تحلیل پروفایل بیان ژن بسیار زیاد بیشتر از خود آزمایش اولیه زمان میبرد.
بسیاری از محققین روشهای مختلف آماری و تحلیل دادهی اکتشافی را قبل از انتشار نتایج پروفایل بیان ژن، استفاده میکنند، و تلاشهایشان را با بایوانفورماتیست ها یا دیگر متخصصان در ریزآرایهی دیانای هماهنگ میکنند. یک طراحی آزمایش خوب، تکرار کافی زیستی و پیگیری آزمایش، نقشهای مهمی در موفقیت آزمایشهای پروفایل بیان ژن دارند.
منابع
- ↑ "Microarrays Factsheet". Retrieved 2007-12-28.
- ↑ Suter L, Babiss LE, Wheeldon EB (2004). "Toxicogenomics in predictive toxicology in drug development". Chem. Biol. 11 (2): 161–71. PMID 15123278. doi:10.1016/j.chembiol.2004.02.003.
- ↑ Magic Z, Radulovic S, Brankovic-Magic M (2007). "cDNA microarrays: identification of gene signatures and their application in clinical practice". J BUON. 12 Suppl 1: S39–44. PMID 17935276.
- ↑ Cheung AN (2007). "Molecular targets in gynaecological cancers". Pathology. 39 (1): 26–45. PMID 17365821. doi:10.1080/00313020601153273.
- ↑ Mirza SP, Olivier M (2007). "Methods and approaches for the comprehensive characterization and quantification of cellular proteomes using mass spectrometry". Physiol Genomics. 33 (1): 3–11. PMC 2771641 Freely accessible. PMID 18162499. doi:10.1152/physiolgenomics.00292.2007.
- ↑ Hebert AS, Richards AL, et al. (2014). "The One Hour Yeast Proteome". Mol Cell Proteomics. 13 (1): 339–347. doi:10.1074/mcp.M113.034769.
- ↑ Chen JJ (2007). "Key aspects of analyzing microarray gene-expression data". Pharmacogenomics. 8 (5): 473–82. PMID 17465711. doi:10.2217/14622416.8.5.473.
- ↑ Jaskowiak, Pablo A; Campello, Ricardo JGB; Costa, Ivan G (24 January 2014). "On the selection of appropriate distances for gene expression data clustering". BMC Bioinformatics. 15 (Suppl 2): S2. PMC 4072854 Freely accessible. PMID 24564555. doi:10.1186/1471-2105-15-S2-S2.
- ↑ Dai M, Wang P, Boyd AD, et al. (2005). "Evolving gene/transcript definitions significantly alter the interpretation of GeneChip data". Nucleic Acids Res. 33 (20): e175. PMC 1283542 Freely accessible. PMID 16284200. doi:10.1093/nar/gni179.
- ↑ Alberts R, Terpstra P, Hardonk M, et al. (2007). "A verification protocol for the probe sequences of Affymetrix genome arrays reveals high probe accuracy for studies in mouse, human and rat". BMC Bioinformatics. 8: 132. PMC 1865557 Freely accessible. PMID 17448222. doi:10.1186/1471-2105-8-132.
- ↑ Curtis RK, Oresic M, Vidal-Puig A (2005). "Pathways to the analysis of microarray data". Trends Biotechnol. 23 (8): 429–35. PMID 15950303. doi:10.1016/j.tibtech.2005.05.011.
- ↑ Couzin J (2006). "Genomics. Microarray data reproduced, but some concerns remain". Science. 313 (5793): 1559. PMID 16973852. doi:10.1126/science.313.5793.1559a.