پرتودرمانی
پرتودرمانی یا رادیوتراپی (به انگلیسی: radiotherapy) یکی از مهمترین شاخههای فیزیک پزشکی است. پرتودرمانی به درمان بیماری با استفاده از پرتوهای نافذ مانند پرتوهای ایکس و امواج آلفا و موج بتا و گاما که یا از دستگاه تابیده میشوند یا از داروهای حاوی مواد نشاندار شده ساطع میشوند گویند.
| پرتودرمانی | |
|---|---|
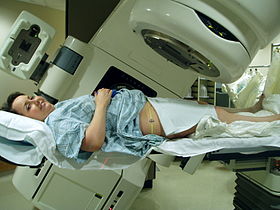 یک دستگاه شتابدهندهٔ لیناک C-LINAC ساخت واریان مدیکال سیستمز، و نحوهٔ قرار گرفتن بیمار برای پرتو درمانی لگن. | |
| ICD-10-PCS | D |
| ICD-9-CM | ۹۲٫۲-۹۲٫۳ |
| سرعنوانهای موضوعی پزشکی | D011878 |
| OPS-301 code | ۸–۵۲ |
| مدلاین پلاس | ۰۰۱۹۱۸ |
پرتودرمانی استفاده از پرتوهای یونساز برای از بین بردن یا کوچک کردن بافتهای سرطانی است. در این روش در اثر آسیب DNA، سلولهای ناحیه درمان (بافت هدف) تخریب و ادامه رشد و تقسیم غیرممکن میشود؛ اگرچه پرتو علاوه بر سلولهای سرطانی به سلولهای سالم نیز آسیب میرساند ولی اکثر سلولهای سالم بهبودی خود را دوباره بهدست میآورند. هدف از پرتو درمانی از بین بردن حداکثر سلولهای سرطانی با حداقل آسیب به بافتهای سالم است.
کاربرد اصلی پرتودرمانی در معالجه یا تقلیل امراض سرطانی میباشد.[۱]
دیگر کاربردهای پرتودرمانی: از بین بردن سلولهای سرطانی و ضایعات ارگانهای مختلف، بازتوانی و بهبود اعضای بدن بیمار (همچون کبد، کلیه، پروستات)، پیشگیری گسترش ضایعات اعضا و کاهش علائم بیماری (همانند درد).
دستگاهها و ابزارهای مختلف و گوناگونی برای درمان و توانبخشی بیمار توسط مهندسان پزشک ساخته و در اختیار پزشکان قرار گرفتهاست. یکی از این دستگاههای مهم و پرکاربرد رادیوتراپی یا پرتودرمانی میباشد. به بیانی دیگر پرتودرمانی، استفاده از اشعه پر انرژی (معمولاً اشعه X) به منظور از بین بردن سلولهای سرطانی و ضایعات ارگانهای مختلف میباشد. بهطور کلی رادیوتراپی را به ۳ قسمت رادیوتراپی خارجی، رادیوتراپی داخلی (براکی تراپی) و رادیوتراپی سیستمیک تقسیم میکنند. سلولهای سرطانی در مقایسه با سلولهای سالم به رادیو تراپی حساسیت بیشتری نشان میدهند و در نتیجه تعداد بیشتری از آنها از بین خواهند رفت البته رادیوتراپی بر سلولهای سالم ناحیه درمان نیز تأثیر میگذارد اما آنها برخلاف سلولهای سرطانی معمولاً بهبود یافته یا به سرعت خود را ترمیم میکنند. رادیوتراپی همچنان برای پیشگیری گسترش ضایعات اعضا و برای کاهش علائم بیماری (همانند درد) نیز به کار برده میشود. اصولاً در این دستگاهها برای شناسایی و مکان یابی تومور و بافت مورد نظر برای دریافت پرتو از انواع مختلف پرتونگاری استفاده میگردد که شاید بتوان مرسومترین آنها را پرتونگاری مقطعی تخمینی (CT)، تصاویر رزونانس مغناطیسی (MRI) و اخیراً پرتونگاری مقطعی نشر پوزیترون (PET) معرفی نمود. حال پس از شناسایی موقعیت بافت مورد نظر بایستی مرحله شبیهسازی را شروع نمود که بر اساس آن آناتومی بیمار برنامهریزی میشود. استفاده از پرتو در درمان سرطان یک فرایند پیچیدهاست که در بر گیرنده متخصصان آموزش دیده و تعداد زیادی از عوامل به هم پیوستهاست. متخصصین رادیوتراپی انکولوژی، متخصصین فیزیک پزشکی، دزیمتریست و متخصصین رادیوتراپی (پرتو پزشکی) سالها دنبال لوازم و ابزار که به این فرایند، بهخصوص در موقعیت یابی تومور، برنامه درمانی، اجرای درمان، و تحقیق کمک کنند، میگشتند. دقت در رادیوتراپی بسیار مهم است زیرا نتایج بالینی و تجربی نشان میدهند که کنترل تومور و پاسخ نرمال بافت میتواند یک عامل مهم درمقدار (دز) پرتو افشانی باشد و بنابراین، تغییرات کوچک در دز درمانی میتواند منجر به نتایج بزرگی در پاسخ تومور یا بافت نرمال شود. به علاوه، دزهای تجویز شده درمانی تومور معمولاً الزاماً به دزی که برای بافت نرمال قابل تحمل است نزدیک است. بنابراین برای درمان بهینه، دز پرتوافشانی باید با دقت بسیار بالا انجام شود. یک میزان ±۵٪ توسط کمیسیون بینالمللی سنجش و واحدهای پرتو افشانی (ICRU) پیشنهاد شدهاست.
نزدیک دو سوم از بیماران سرطانی در جریان مداوای خود از پرتودرمانی استفاده میکنند. در سال ۲۰۰۴، این تعداد در آمریکا به ۱ میلیون نفر رسید. در این میان، سرطان پروستات، سرطان ریه، و سرطان سینه ۵۶٪ معضلات را تشکیل میدادند[۲].
پیشینه
ویرایشطی دو دهه نخست سده بیستم، رشته رادیوتراپی انکولوژی تغییرات چشمگیری را پشت سر گذاشتهاست. در آن زمان متخصصین رادیوتراپی انکولوژی برای برنامهریزی و درمان بیماران با استفاده از آنچه روش دو بعدی (2D) نامیده میشد، آموزش دیده بودند. این روش تأکید داشت بر استفاده از یک شبیه ساز مرسوم اشعه ایکس برای طراحی پرتالهای پرتویی که بر اساس تکنیکهای ترکیب اشعهای استاندارد و استفاده از بوکمارکهای استخوانی تجسم شده بر روی صفحه رادیوگرافی، هستند. این روش در حالی که هنوز توسط برخی کلینیکها استفاده میشود بهطور گسترده با یک روش سه بعدی(3D) در کلینیکهای پرتو درمانی مدرن جایگزین شدهاست. با معرفی سیستمهای برنامهریزی درمان 3D تجاری در اوایل دهه ۱۹۹۰ این روش امکانپذیر شد. در مقابل روش 2D، برنامهریزی درمان 3D بر یک روش شبیهسازی مجازی بر پایه تصویر برای تعیین حجم تومور و اعضای مهم در خطر برای بیمار خاص تأکید دارد. این فرایند 3D جدید برای متخصصین رادیوتراپی انکولوژی جهت تشخیص حجم و اعضای هدف را که در خطر هستند، با دقتی بسیار بالاتر از قبل، تقاضاهای جدیدی را ایجاد کرد. و همچنین برای متخصصین فیزیک پزشکی برای فراهم کردن فرایندهای با کیفیت مطمئن(QA) و مؤثر برای اطمینان بخشیدن به استفاده ایمن از این برنامهریزی جدید بر اساس تصویر و روش کنترل درمان کامپیوتری.
مشخص نیست که چه کسی برای نخستین مرتبه در تاریخ از پرتوهای یونیزان برای مقاصد درمانی استفاده کرد، اما یکی از اولین کوششهای اینچنینی متعلق به سال ۱۸۹۶ است که ویکتور دسپن [پانویس ۱] بهطور ناموفقی سعی در درمان سرطان معده با پرتوهای ایکس نمود.[۳] در آن زمان پرتوها دارای انرژی کافی نبودند و لذا پرتودرمانی را فقط برای غدههای سطوحی امکانپذیر مینمودند. این وضعیت البته با ابداع تجهیزات ویژه ۲۰۰ کیلوولتی در سال ۱۹۲۲ میلادی دچار دگرگونی شد.[۴] در همان سال، یک جراح اتریشی بنام لئوپولد فرویند[۵] چگونگی درمان یک خال گوشتی توسط پرتوهای اشعه ایکس را برای نخستین بار به انجمن پزشکی وین نشان داد.[۶]
ابزار نگهداری و جابجایی بیمار
ویرایشتغییر مکان دقیق روزانه بیمار در موقعیت درمان و کاهش حرکت بیمار در طول درمان جهت اینکه دز تجویز شده دقیقاً ارائه شود و توزیع دز طراحی شده حاصل گردد، ضروری است.همانطور که در این بخش خواهیم دید سیستمهای مدرن تغییر موقعیت و عدم تحرک طوری طراحی شدهاند که بتوانند متصل شوند به تختهای درمان و شبیه سازی،بطوریکه ابزار عدم تحرک و بیمار ثابت شده باشند در سیستم هماهنگکننده ماشین درمان.زمانی که ابزار عدم تحرک در یک مکان خاص قفل شود ،بیمار هم تراز سیستم عدم تحرک خواهد بود.نتیجه نهایی این است که مجموعهای از هم پایهها که از شبیه ساز CT بهدست آمدهاستو در فرایند شبیهسازی مجازی استفاده شدهاست و میتواند هم پایه شود با مرکز اتاق درمان. سایتهای اناتومیک معمولاً عدم تحرک را در تشعشع درمانی در سروگردن، سینه، قفسه سینه-مری، شانهها و دستها، مناطق لگن (به خصوص در افراد چاق)، و اندام چرخیده شده در جهت خلاف، مورد استفاده قرار میدهند.
انواع پرتودرمانی
ویرایشپرتودهی ممکن است توسط دستگاهی خارج از بدن ( رادیوتراپی خارجی ) یا توسط منبع پرتو در داخل بدن ( رادیوتراپی داخلی ) یا توسط مواد رادیواکتیو باز درداخل بدن انجام شود ( رادیوتراپی سیستمیک ) . نوع پرتودهی به نوع تومور، تحمل بافتهای سالم اطراف محل آن، مسافتی که پرتو باید در داخل بدن طی کند همچنین به سلامت عمومی بیمار، تاریخچه بیماری و اینکه آیا بیمار از روشهای دیگر درمان استفاده خواهد کرد یا نه و مجموعهای عوامل دیگر بستگی دارد . در بیشتر بیماران از روش پرتودرمانی خارجی و در تعدادی از بیماران از سه روش پرتو درمانی خارجی، داخلی، سیستمیک همراه با هم یا جداگانه استفاده میشود.
پرتو درمانی با دستگاه سایبر نایف: سایبر نایف جدیدترین روش درمان تومورهای سرطانی به صورت جراحی بسته میباشد و کاملاً میتواند جایگزینی برای عمل جراحی باز باشد با این تفاوت که درمان با این روش بدون درد، خونریزی و کمترین عوارض جانبی برای بیماران سرطانی میباشد. علاوه بر این درصد موفقیت و نابود کردن تومورهای سرطانی با این روش بسیار بالاست. بتازگی یک دستگاه سایبر نایف در یکی از مراکز درمانی شیراز کارگذاری و در حال بهره برداری می باشد.
رادیوتراپی خارجی: پرتودرمانی یا رادیوتراپی خارجی معمولاً در بیماران سرپایی مورد استفاده قرار میگیرد. در بیشتر این بیماران نیاز به بستری شدن در بیمارستان نیست رادیوتراپی خارجی برای درمان انواع سرطان شامل سرطان مثانه، مغز، پستان، رکتوم، پانکراس، معده، گردن رحم، حنجره، ریه، پروستات و رحم استفاده میشود علاوه بر این رادیوتراپی خارجی ممکن است برای کاهش دردهای متاستاتیک یا مشکلات دیگر ناشی از گسترش تومورها مورد استفاده قرار گیرد.
پرتودرمانی حین جراحی (Intraoperative Radiotherapy): این روش نوعی پرتو درمانی خارجی همراه با جراحی است. IIORT برای درمان تومورهای متمرکز که نمیتوان آنها را بهطور کامل خارج کرد یا ریسک عود مجدد وجود دارد استفاده می¬شود. بعد از خارج کردن تمام یا بیشتر بافت تومورال یک دوز زیاد با انرژی بالا مستقیماً به محل تومور در حین جراحی داده میشود ( بافتهای سالم اطراف به وسیلهٔ شیلدهای مخصوصی حفاظت میشوند ) . بیمار بعد از عمل جراحی در بیمارستان بستری میشود این روش ممکن است در درمان تومورهای تیروئید، gynecological , colorectal روده باریک و لوزالمعده ( پانکراس ) استفاده شود . این روش برای درمان برخی از انواع تومورهای مغز و سارکومای لگن در بزرگسالان تحت بررسی است .
پرتودرمانی تطبیقی سه بعدی 3D Conformal Radiation Therapy : رادیوتراپی تطبیقی برخلاف طرح درمانهای قدیمی سه بعدی است و از کامپیوتر برای هدفگیری دقیق تر تومور استفاده میشود . امروزه بیشتر متخصصین سرطانشناسی از این روش استفاده میکنند . تصاویر سه بعدی CT، MRI، PET ویا SPECT تهیه و به کمک نرمافزارهای مخصوص، پرتوهایی که با شکل تومور مطابقت دارند طراحی میشود . چون در این تکنیک بافت سالم اطراف تومور بهطور وسیع از تشعشع دور است از دوزهای بالاتر برای درمان تومور میتوان استفاده کرد . استفاده از این روش در تومورهای Nasopharyngeal، پروستات ریه، کبد و تومورهای مغزی نتایج بهتری در برداشتهاست .
IMRT) Therapy Intensity-Modulated Radiation) : در این روش که یک نوع رادیوتراپی تطبیقی سه بعدی جدید است معمولاً از پرتوهای x با شدتهای متفاوت برای انتقال دزهای متفاوت پرتو به نواحی کوچک بافت بهطور همزمان استفاده میشود . در این تکنولوژی نیز دزهای بالا به تومور و دزهای کمتر به بافتهای سالم اطراف میرسد . در برخی تکنیکها بیمار دز روزانه بیشتری دریافت میکند و زمان کل درمان کاهش و موفقیت درمان بیشتر میشود . IMRT ممکن است عوارض جانبی درمان را کاهش دهد. پرتودهی در این روش به وسیلهٔ یک شتاب دهنده خطی مجهز به کولیماتور Multileaf انجام میشود(کولیماتور به شکل دادن دقیق پرتوها کمک میکند). با چرخش دستگاه به دور بدن بیمار پرتوها از بهترین زوایا وارد تومور میشوند . پرتوها تا حد امکان بهطور دقیق با شکل تومور تطبیق داده میشوند . چون دستگاه IMRT بسیار تخصصی است مراکز سرطانشناس به ندرت از این وسیله استفاده میکنند . این تکنولوژی جدید برای درمان تومورهای مغزی، سروگردن، حلق بینی، پستان، کبد، ریه، پروستات و رحم مورد استفاده قرار میگیرد . IMRT برای هر بیمار یا هر نوع توموری مورد استفاده قرار نمیگیرد.
پرتودرمانی داخلی( Brachy Therapy ) : در این روش منبع تشعشع که در یک پوشش نگهدارنده کوچک پیچیده شده در داخل تومور یا بسیار نزدیک به آن قرار میگیرد و Implant یا ماده کاشتنی نامیده میشود. مواد کاشتنی ممکن است در شکلهای مختلف مانند سیمهای کوچک، تیوبهای پلاستیکی ( کاتترها ) ribbans ( رشتهای ) کپسول یا به شکل دانهای وجود داشته باشد . مواد کاشتنی مستقیماً در داخل بدن گذاشته میشوند . در رادیوتراپی داخلی ممکن است بیمار نیاز به بستری داشته باشد . رادیوتراپی داخلی معمولاً به یکی از روشهای زیر انجام میشود که هرکدام بهطور جداگانه توضیح داده شدهاست . در هر سه روش از مواد کاشتنی سربسته استفاده میشود .
پرتودرمانی داخل نسجی (Interstitial Rediotherapy): در این روش ماده رادیواکتیو در داخل بافت یا نزدیک محل تومور قرار میگیرد . این روش در درمان تومورهای سر و گردن، پروستات، گردن رحم (Cervix )، تخمدان، پستان، نواحی لگن و اطراف مقعد استفاده میشود . در رادیوتراپی خارجی پستان ممکن است یک دوز بیشتر ( Boost ) به روش داخل نسجی یا خارجی به بیمار داده شود .
پرتودرمانی داخل حفرهای (Therapy Intracavitary): در این روش منبع رادیواکتیو به وسیلهٔ یک اپلیکاتور در داخل بدن قرار میگیرد . این روش معمولاً در درمان تومورهای رحم استفاده میشود . محققان در حال مطالعه و بررسی انواع رادیوتراپی داخلی برای درمان دیگر سرطانها شامل پستان، Bronchial، گردنی، مثانه، دهانی، Tracheal ,Rectal، رحم و واژن هستند.
پرتودرمانی سیستمیک( پزشکی هستهای ): در این روش از مواد رادیواکتیو مانند I131 Strontium89. به صورت خوراکی یا تزریقی استفاده میشود . این روش درمانی گاهی برای درمان سرطان تیروئید و لنفوم غیر هوچکینی بزرگسالان استفاده میشود . محققان در حال بررسی موادی هستند که بتواند برای درمان دیگر انواع سرطان استفاده شود .
منابع انرژی در رادیوتراپی خارجی
ویرایشمنابع پرتودهی مورد استفاده در رادیوتراپی خارجی ممکن است شامل انواع زیر باشد :
اشعه گاما یا x : این پرتوها از نوع تشعشع الکترومغناطیس محسوب میشوند، ولی طریقه تولید آنها متفاوت است . پرتوهای x به وسیلهٔ دستگاهی به نام شتاب دهنده خطی تولید میشوند . پرتوهای با انرژی پایین در تخریب سلولهای سرطانی سطحی و پرتوهای با انرژی بالاتر در درمان تومورهای عمقی تر بکار میرود. پرتوهای x میتوانند یک ناحیه بزرگ را مورد تشعشع قرار دهند . پرتوهای گاما از رادیو ایزوتوپهایی مثل ایدیدیوم Ir و CO60 منتشر میشوند . هر عنصر در یک زمان خاص واپاشی و میزان متفاوتی از انرژی را آزاد میکند که بر نفوذ آن به داخل بدن مؤثر است . در واپاشی کبالت پرتوی گاما منتشر میشود که در درمان با knife Gamma نیز مورد استفاده قرار میگیرد.
پرتوهای ذرهای ( Particle beams ): در این روش از ذرات هستهای پر انرژی به جای فوتون استفاده میشود . این روش درمانی، رادیوتراپی ذرهای یا تشعشع ذرهای نامیده میشود . تشعشعات ذرهای به وسیله شتاب دهندههای خطی، سنکروترن و سیکلوترون تولید میشود. ذرات شتابدار عبارتند از : الکترون که به وسیله تیوب اشعه X تولید میشود، نوترونها که به وسیله عناصر رادیواکتیو و تجهیزات مخصوص تولید میشوند. یونهای سنگین مثل پروتونها، هلیوم و ذرات باردار کوچک یعنی مزون که به وسیله شتابدهنده و یک سیستم مغناطیسی تولید میشوند. برخلاف پرتوهای ایکس و گاما، پرتوهای ذرهای قدرت نفوذ کم دارند . بنابراین از این پرتوها معمولاً برای درمان تومورهای سطحی یا زیر جلدی استفاده میشوند .
درمان با پرتوی پروتون ( Proton beam therapy ): در این روش از پرتوهای پروتونی استفاده میشود که انرژی خود را در یک ناحیه کوچک ( Bragg peak ) از دست میدهند. در این ناحیه دزهای بالا بر روی تومور با حداقل آسیب به بافتهای نرمال متمرکز میشود . پروتون درمانی فعلاً در مراکز محدودی در ایالات متحده استفاده میشود . این شیوه برای درمان تومورهایی که عمل جراحی مشکل یا پر مخاطره است به کار میرود . تحقیقات کلینیکی برای استفاده از این روش در درمان ملانومای چشم، Retinoblastoma ( یک نوع تومور چشمی که بیشتر در اطفال زیر 5 سال اتفاق می افتد ) سارکومای عضلات مخطط، برخی انواع تومورهای سر و گردن، پروستات، مغز و ریه در حال انجام است.
درمان با پرتوی کربن ( carbon beam therapy ): در این روش از پرتوهای یونهای کربن استفاده میشود که انرژی خود را در یک ناحیهٔ کوچک (Bragg peak ) همانند پروتون از دست میدهند، و حداقل آسیب به بافتهای سالم را در پی خواهد داشت. به علت هزینهٔ بالای شتاب دهندههای تولیدکنندهٔ یونهای کربن با سرعت بالا، به کارگیری این روش درمانی با محدودیت زیادی روبرو است.
منابع انرژی مورد استفاده در پرتو درمانی داخلی
ویرایشمنابع تشعشع مورد استفاده در رادیوتراپی داخلی عبارتند از : ایزوتوپهای رادیواکتیو مانند (I131 ) و Sr89، فسفر ،palladium، سزیم، ایریدیوم، فسفات یا کبالت، منابع دیگری هم در دست بررسی هستند .
Stereo tactic radiosurgery & Stereo tactic Rodiotherapy : در روش اول از یک دوز بالا برای تخریب بافت تومورال در مغز استفاده میشود . سر بیمار در یک قالب مخصوص که به جمجمه متصل است قرار میگیرد . از قالب به منظور تابش به خط مستقیم به تومور سر بیمار استفاده میشود . تابش دقیقاً در ناحیه مورد نظر خواهد بود. این روش بافتهای اطراف تومور عموماً از آسیب در امان خواهند ماند . این شیوه به سه صورت انجام میگیرد : روش متداول استفاده از فوتونهای با انرژی زیاد شتاب دهنده خطی که Linac -based stereo tactic RT نامیده میشود. در دومین روش از پرتوی گامای CO60 و در روش سوم از پرتوهای ذرات باردار سنگین مثل پروتونها و یونهای هلیوم Stereo tactic استفاده میشود . این روش اکثراً در درمان تومورهای کوچک خوش خیم یا بد خیم مغز مثل مننژیوما، و تومور هیپوفیز همچنین در درمان بیماریهای دیگر مثل پارکینسون، صرع، تومورهای متاستاتیک مغز ( تومورهایی که از قسمتهای دیگر بدن انتشار یافتهاند )، به صورت منفرد یا همراه با رادیوتراپی تمام مغز مورد استفاده قرار میگیرند.
Stereo tactic Radiotherapy : در این روش از همان شیوه مورد استفاده در روشهای قبل ولی با دوزهای پایین در تعداد جلسات متعدد استفاده میشود . دزهای کم و تعداد جلسات زیاد نتیجه را بهبود بخشیده، عوارض اشعه را به حداقل میرساند. این روش برای درمان تومورهای مغزی با همان روشی که در قسمتهای دیگر بدن بکار میرود، استفاده میشود . در تحقیقات بالینی سودمندی این دو شیوه به صورت منفرد یا همراه با دیگر روشهای پرتو درمانی در حال بررسی است .
دسته بندی ابزار پرتودرمانی
ویرایشابزار شبیه سازی: جهت کمک به تجسم و تعیین اندازه تومور برای بهدست آوردن سنجش ضخامتها و موقعیت یابی و درمان تومور.
ابزار برپایی و خودداری انباشتگی بیمار: به منظور تغییر مکان دقیق روزانه بیمار در طول مدت درمان و کاهش حرکت بیمار در طول درمان تا توزیع دز تجویز شده بهطور دقیقی انجام گیرد.
ابزار شکل دهی: به منظور حذف اشتباهات بالقوه در ردیابی دستی، بزرگ نمایی و واژگونی تصویر استفاده میگردد.
ابزار اطمینان کیفیت: ارزیابی کمی از عدم تحرک و تغییر موقعیت بیمار برای تصویربرداری روزانه دارند.
روشهای پرتودهی
ویرایشروشهای مختلفی برای پرتودهی و انتقال اشعه با قدرت نفوذ متفاوت وجود دارد، علاوه بر این تعدادی از روشهای پرتو دهی میتواند بهطور دقیق و کنترل شده برای درمان ناحیه کوچکی از بافت بدون آسیب به بافت و اندامهای اطراف استفاده شود، درحالیکه برای درمان نواحی بزرگتر از انواع دیگر پرتو استفاده میشود. مثلاً در مواردی از دستگاههای بزرگی که اشعه x و گاهی اشعه گاما یا الکترون تولید میکنند استفاده میشود، بیمار را به دقت بر روی تخت درمان میخوابانند آنگاه دستگاه دقیقاً بالای منطقهٔ سرطانی تنظیم میشود.
مواقع استفاده از پرتودرمانی
ویرایشرادیوتراپی ممکن است برای درمان انواع تومورهای جامد شامل تومورهای مغز، پستان، دهانه رحم (Cervix )، حنجره، ریه، پانکراس، پروستات، پوست، نخاع، معده، رحم یا سارکومای بافت نرم و استخوان درمان لوسمی و لنفوم (تومور سیستم لنفاوی) و برخی تومورهای خوش خیم به کار رود. مقدار دز مورد استفاده در پرتودرمانی به نوع تومور و بافت یا اندامهای درمعرض آسیب بستگی دارد. برای بعضی از تومورها، پرتودهی به نواحی غیرتومورال برای جلوگیری از رشد مجدد سلولهای سرطانی صورت میگیرد. این تکنیک، پرتو درمانی پیشگیریکننده (Prophylactic) نامیده میشود. رادیوتراپی همچنین میتواند به کاهش علائم بیمار مثل درد ناشی از گسترش سرطان به استخوان یا سایر بافتهای بدن کمک کند. این تکنیک رادیوتراپی تسکینی (Palliative) نامیده میشود. بهطور کلی در تعدادی از بیماران هدف از درمان، تخریب کامل تومور و بعضی بیماران کوچک کردن تومور یا کاهش علائم بیماری (مانند درد) است. نیمی از بیماران سرطانی پرتودرمانی میشوند. پرتودرمانی ممکن است به صورت منفرد یا همراه با دیگر روشهای درمان (شیمی درمانی یا جراحی) مورد استفاده قرار گیرد. حتی در بعضی موارد ممکن است بیش از یک روش پرتودرمانی به کار گرفته شود.
اندازهگیری دوز تشعشع
ویرایشمقدار انرژی جذب شده در واحد جرم ماده دز جذبی یا دوز تشعشع نامیده میشود . تا قبل از سال 1985 واحد دز جذبی، راد (rad ) بود امروزه از واحد گری ( Gy) استفاده میشود . یکگری برابر با rad 100 است ( 1cGy = 1 rad ) . دوز قابل تحمل بافتهای مختلف متفاوت است برای مثال کبد میتواند یک دز مجموع cGy3000 را تحمل کند در صورتی که کلیهها قدرت تحمل cGy 1800 دارند . دز مجموع معمولاً به دزهای کوچکتر در تعداد جلسات معین که به صورت روزانه داده میشود، تقسیم میشود. این روش باعث افزایش تخریب سلولهای سرطانی با حداقل آسیب به بافت سالم میشود. برای نشان دادن میزان آسیب سلولهای سرطانی در مقایسه با سلولهای سالم از یک ضریب به نام نسبت درمانی (therapeutic ratio ) استفاده میشود.
پرتوهای LET Low و پرتوهای LET High
ویرایشLET معرف میزان انرژی به جا مانده از پرتو در هنگام عبور از بافت است. با جذب انرژی بیشتر سلولهای بیشتری از بین میروند . LET پرتوها متفاوت است. برای مثال پرتوهای x، گاما و الکترونها Low LET و poins و نوترونها، یونهای سنگین LET Highمیباشند. تحقیق و بررسی دربارهٔ پرتوهایLET High در حال انجام است . هزینه سنگین این تجهیزات و آموزشهای تخصصی مورد نیاز، استفاده از این پرتوها را به مراکز اندکی در ایالات متحده آمریکا محدود کردهاست.
طراحان درمان در پرتو درمانی
ویرایشمجموعه کارکنان هر مرکز رادیوتراپی به طراحی و درمان بیمار کمک میکنند. تیم پرتو درمانی شامل رادیوتراپیست، دوزیمتریست ( شخصی که دوز کامل و دقیق پرتو را مشخص میکند )، فیزیست (فردی که کنترل دستگاه برای انتقال مقدار صحیح پرتو به محل تومور در بدن را انجام میدهد) و پرتوکار میباشد. معمولاً پرتو درمانی یک قسمت از درمان بیمار را شامل میشود در درمان تکمیلی معمولاً از شیمی درمانی استفاده میشود. رادیوتراپیست Radiation oncologist، از همکاری با متخصص سرطانشناس اطفال، جراح و رادیولوژیست ( پزشک متخصص در تهیه و تفسیر گرافیهای اندامهای بدن ) پاتولوژیست ( پزشک متخصص آسیبشناسی ) سود میبرد .
طراحی درمان
ویرایشدر هر بیمار، طراحی درمان برای محافظت بافتهای سالم تا حد امکان انجام میشود. بیمار باید قبل از شروع دوره رادیو تراپی در جلسهٔ طرح درمان شرکت کند. بیماری که با رادیو تراپی تحت درمان قرار میگیرد باید طرح درمان منحصر به فردی داشته باشد. به دلیل تنوع روشهای پرتو دهی طراحی درمان یک گام اولیه و مهم برای درمان هر بیمار تحت پرتو درمانی است . قبل از پرتو درمانی گروه رادیوتراپی میزان و نوع پرتو را مشخص خواهند کرد . اگر بیمار باید تحت پرتو درمانی خارجی قرار گیرد رادیوتراپیست از روشی به نام Simulation (شبیه سازی) برای مشخص کردن هدف پرتویی استفاده میکند در طول انجام Simulation بیمار به حالت آرام بر روی تخت قرار میگیرد و محدوده درمان توسط Simulation مشخص میشود . شبیهسازی همچنین ممکن است شامل CT یا سایر روشهای تصویر برداری برای کمک به پرتوکار در جهت طراحی پرتو دهی باشد . Simulation ممکن است باعث تغییراتی در طراحی درمان و در نتیجه محافظت بیشتر بافت سالم از تشعشعات شود. نواحی که باید تحت پرتودهی قرار گیرند توسط یک مارکر دائمی یا موقتی (ناتوی کوچک) مثل خالکوبی مشخص میشود. این نشانهها در اولین جلسه درمان برای تعیین محل دقیق پرتو دهی به کار میرود . بسته به نوع پرتو درمانی، پرتوکار ممکن است از Mold یا وسایل دیگر برای بی حرکت نگه داشتن بیمار در طول درمان استفاده کند. این وسایل معمولاً از فوم، پلاستیک یا گچ ساخته میشوند . در بعضی موارد پرتوکار شیلدهایی را به منظور جلوگیری از نفوذ پرتو به ارگان و بافتهای اطراف محل درمان مورد استفاده قرار میدهد. زمانی که شبیهسازی کامل شد تیم رادیوتراپی برای تصمیمگیری دربارهٔ مقدار دوز مورد نیاز و چگونگی رساندن آن به محل مورد نظر و درمانهایی که دربارهٔ بیمار باید انجام گیرد تصمیمگیری میکند.
مکان یابی تومور و ابزار شبیهسازی درمان
ویرایشابزار و وسایل در این ردیف جهت کمک به تجسم کردن و تعیین کردن اندازه تومور در مقابل با هندسه درمان (مکان یابی حجم هدف) و برای بهدست آوردن سنجش ضخامتها و حد فاصل بدن بیمار طراحی شدهاند.در گذشته، مکان یابی حجم هدف معمولاً با آزمایش فیزیکی و استفاده از ابزاری به نام شبیه ساز اشعه ایکس،که توانایی عکس رادیوگرافی و رادیوسکوپی را در یک ماشین که هندسه درمان حقیقی فرد را تقلید میکند، ترکیب میکند،به دست می آمد.فرایند شبیهسازی خودش میتواند با دیگر مطالعات تجسمی تشخیصی که شامل پرتونگاری مقطعی تخمینی (CT)، تصاویر رزونانس مغناطیسی (MRI)، و اخیراً، پرتونگاری مقطعی نشر پوزیترون(PET) تکمیل شود. ابزاری که برای کمک کردن به فرایند شبیهسازی مرسوم استفاده میشود شامل یک توری ثابت رادیوپک که بر اساس آناتومی بیمار برنامهریزی میشود و اجازه میدهد که ابعاد حجم درمان از طریق فیلمهای طرح شبیهسازی شده تشخیص داده شود، میباشد.نمونه دیگر ابزار ساخته شده در فرایند موقعیت یابی حجم هدف 2D حلقههای بزرگی هستند که در میدان اشعه تابیده شده قرار داده میشوند و میلههای سرتیزی که میتوانند در دهانههای بدن وارد شوند، مانند واژن برای سرطان سرویکس یا داخل مقعد برای سرطان پروستات.سر تیز میتواند بهطور واضح در فیلمهای شبیهسازی شده یا فیلمهای پرتال درمانی تجسم یابد و ارزیابی تفاوتهای زمینه درمان را اجازه دهد. باید توجه داشت که نسل جدیدی از شبیه سازهای مرسوم جدیداً پیشرفت کرده اند(شکل 32)، بهطوریکه سیستم تشدیدکننده تصویر با یک ردیاب صفحه تخت بی ریخت جایگزین میشود. این ابزار تصاویر دیجیتالی با وضوح بالا و شکستگی آزاد به علاوه CT پرتو مخروطی تولید میکند.
A،چرخش دورانی: B، فاصله محور مبدا: C، چرخش کولیماتور: D، بزرگکننده تصویر(عرضی)،Eبزرگکننده تصویر (طولی)،F بزرگکننده تصویر (محوری)،G میز بیمار(عمودی)،H میز بیمار(عرضی)،Kچرخش میز بیمار حول ایزوسنتر،J چرخش میز بیمار حول محور،Lکاست فیلم،Mبزرگکننده تصویر.اجزا نشان داده نشده شامل تصویر سایز زمینه،دیافراگمهای پرتو و فاصله منبع-سینی میشود.
حساسکنندهها و محافظتکنندههای پرتویی
ویرایشحساس و محافظتکنندههای پرتویی مواد شیمیایی هستند که پاسخ سلول به تشعشع را تغییر میدهند . حساسکنندههای پرتویی(Radiosensitizers) داروهایی هستند که سلولهای سرطانی را نسبت به تشعشع حساستر میکنند . برخی از این ترکیبات تحت مطالعه هستند . علاوه بر این تعدادی از داروهای ضد سرطان مثل 5-flaurouracil و Cisplatin سلولهای سرطانی را نسبت به رادیوتراپی حساستر میکنند . محافظتکنندههای پرتویی که Radioprotectors هم نامیده میشوند داروهایی هستند که سلولهای سالم را از آسیب ایجاد شده توسط تشعشع محافظت میکنند . این مواد ترمیم سلولهای غیر سرطانی آسیب دیده را تسهیل میکنند . Amifostine تنها دارویی است که توسط اداره دارو و غذای ایالات متحده آمریکا (FDA ) به عنوان محافظتکننده پرتویی تأیید شدهاست . این دارو به کاهش خشک شدگی دهان ناشی از دریافت تشعشع زیاد در تومور غده پاروتید ( بنا گوشی ) کمک میکند . مطالعات دیگری برای تشخیص مؤثر بودن Amifostine در درمان سرطانهای دیگر در حال انجام است.
رادیو داروها (Radiopharmaceuticals) و چگونه استفاده آنها
ویرایشاین داروها که تحت عنوان رادیو نوکلئوتیدها شناخته میشوند داروهای رادیواکتیوی هستند که برای درمان انواع سرطان شامل تومور تیروئید، تومور عود کرده قفسه سینه و تومور متاستاتیک استخوان استفاده میشوند . بیشترین استفاده مربوط به Samarium153 و Strontium89 میباشد . این داروها به وسیلهٔ FDA برای کاهش درد متاستاتیک استخوان تأیید شدهاست . هردو دارو از طریق تزریق داخل وریدی و معمولاً در بیماران سرپایی مورد استفاده قرار میگیرند. بعضی مواقع این داروها به همراه رادیوتراپی خارجی استفاده میشود . انواع دیگر رادیو نوکلئوتیدها P32، Rhodium186 و گالیم نیترات میباشد داروهای دیگری نیز تحت مطالعه و بررسی هستند.
شیوههای جدید رادیوتراپی
ویرایشگرما درمانی ( استفاده از حرارت ) همراه با رادیوتراپی در حال مطالعه است محققان دریافتهاند، ترکیب حرارت و پرتو میتواند میزان پاسخ دهی بعضی تومورها را افزایش دهد محققان همچنین در حال مطالعه دربارهٔ استفاده از آنتی بادیهای نشان دار برای انتقال تشعشع بهطور مستقیم و صحیح به محل تومورند که رادیو ایمونوتراپی ( Radio immunotherapy ) نامیده میشود. آنتی بادیها، پروتئینهای مخصوصی هستند که به وسیلهٔ بدن در پاسخ به حضور آنتی ژنها ( موادیکه به عنوان عوامل خارجی توسط سیستم ایمنی در نظر گرفته میشوند ) ساخته میشوند. این آنتی بادیها میتواند در آزمایشگاه و در اتصال با مواد رادیواکتیو (طی روندی که نشان دار کردن نامیده میشود ) ساخته شوند. این مواد بداخل بدن تزریق و بهدنبال سلولهای سرطانی تخریب شده میگردند. این روش میتواند ریسک آسیب پرتویی سلولهای سالم را به حداقل برساند . موفقیت در این تکنیک به تشخیص صحیح ماده رادیواکتیو و مشخص کردن دز مؤثر و ایمن مورد استفاده در این شیوه بستگی دارد. استفاده از رادیو ایمونوتراپی در برخی از تومورها شامل لوسمی، NHL، Colorectal و تومورهای کبد، ریه، مغز، پروستات، تیروئید، پستان، تخمدان و لوزالمعده تحت بررسی است.
مقایسهای بین پرتودرمانی و عمل جراحی در یک مورد خاص
ویرایشمثلاً در یکی از موارد هم رادیو تراپی و هم عمل جراحی رادیکال پروستاتکتومی برای درمان اصلی سرطان پروستات کاربرد دارد که هر کدام دارای عوارض جانبی خودشان میباشند. معایب و مزایای این دو روش درمانی زیاد با هم تفاوت ندارند. همچنین از آنجایی که تأثیرات نسبی این درمانها مشابه میباشند، بیمار مبتلا به سرطان پروستات باید خودش در انتخاب هریک از این دو نوع روش درمانی آزاد باشد. بعضی از افراد، عمل جراحی را ترجیح میدهند و دوست دارند که تومور سرطانی از بدنشان بیرون آورده شود، اما عدهای دیگر، رادیوتراپی را ترجیح میدهند. عمل جراحی برای کسانی که به بیماریهای قلبی و ریوی مبتلا هستند مناسب نمیباشد و بنابراین به آنها توصیه میگردد که از رادیوتراپی استفاده نمایند.
عوارض رادیوتراپی در این مورد: دردرمان رادیوتراپی، عدم کنترل ادراری معمولاً دیده نمیشود و گرچه اختلال در نعوظ گاهی رخ میدهد اما خیلی کمتر از موا ردی است که بعد از عمل جراحی رادیکال پروستاتکتومی دیده میشود با این حال، از آنجایی که غیرممکن است که اشعه رادیو تراپی دقیقاً فقط به پروستات تابیده شود. اثرات موقتی بر روی مثانه و راست روده ممکن است ایجاد شود. اکثر بیماران بعد از رادیوتراپی دچار علایم التهاب مثانه ( سوزش و تکرر ادرار ) و اسهال میگردند. گاهی ممکن است در ادرار یا مدفوع، خون دیده شود. این علایم معمولاً بعد از چند هفته که رادیوتراپی به اتمام رسید، برطرف میشوند. در بعضی موارد، علایم بیماری باقیمانده و خیلی به ندرت ممکن است رادیوتراپی باعث ایجاد آسیبهای دایمی به مثانه و روده شود. یک روش دیگر برای رادیوتراپی، استفاده از یک عمل جراحی و قرار دادن دانههای حاوی مواد رادیو اکتیو در داخل پروستات میباشد. از این روش زیاد استفاده نمیشود، اما با بهبودهایی که در این روش ایجاد شدهاست، دوباره استفاده از آن در حال افزایش پیدا کردن است. به این روش اصطلاحاً "براکی تراپی" (Brachy Therapy) گفته میشود.
عوارض جانبی پرتودرمانی
ویرایشباعث سوختگی پوست میشود(مشابه آفتاب سوختگی). معمولاً در طول دوره رادیوتراپی استحمام مجاز نمیباشد. بهطور کلی پرتودرمانی موجب ریزش مو نمیگردد ولی اگر پرتودهی در ناحیه سر باشد میتواند باعث ریزش موی سر گردد.
پرتودرمانی نوین
ویرایشدر پرتو درمانی از شتابدهندههایی ویژه برای تولید الکترون جهت نفوذ به درون بدن بیمار استفاده میشود. از پرتوهای فوتونی پر انرژی نیز استفاده میشود.
برای نمونه میتوان از سیستمهای چاقوی گاما، سایبر نایف، لیناک و توموتراپی نام برد. اما گاهی نیز از تکنیکهای کاشت رادیو ایزوتوپ، همانند برکیتراپی نیز استفاده میگردد.
در روشهای پرتودرمانی نوین نیز از پرتوهای با انرژی بالا از پروتون یا نوترون نیز استفاده میگردد (که به آن پروتون درمانی و درمان با گیراندازی نوترون بور گویند) و استفاده از یونهای سنگینتر نیز در مرحله تحقیقات است.
اشتغال
ویرایشدر سال ۲۰۰۴، ۲۹۹۷۰ متخصص در زمینه پرتودرمانی در آمریکا در حال کار بودند که این تعداد در مقایسه با سال ۲۰۰۳ حدود ۳٪ افزایش داشت.[۲]
جستارهای وابسته
ویرایشمنابع و پانویس
ویرایش- واژههای مصوب فرهنگستان زبان و ادب فارسی
- ↑ The Physics of Radiation Therapy, Faiz M Khan, Lippincott Williams & Wilkins, 3 edition, 2003
- ↑ ۲٫۰ ۲٫۱ «American Society for Radiation Oncology» (PDF). بایگانیشده از اصلی (PDF) در ۲۵ مه ۲۰۱۰. دریافتشده در ۱۰ ژوئیه ۲۰۰۹.
- ↑ Leszczynski K, Boyko S. On the controversies surrounding the origins of radiation therapy. Radiother Oncol. 1997; 42, pp.213-217
- ↑ Robinson RF. The race for megavoltage. X-rays versus telegamma. Acta Oncol. 1995. 34; pp.1055-74
- ↑ Leopold Freund
- ↑ Radiobiology for the Radiobiologist. Eric Hall. 2006. 6ED. ISBN 0-7817-4151-3 pp.5
پیوند به بیرون
ویرایش- (مرکز فیزیک پرتوی ایالات متحده آمریکا) Radiological Physics Center
- What is Gamma-knife بایگانیشده در ۱۹ سپتامبر ۲۰۰۷ توسط Wayback Machine
- Radiation Therapy with Tomotherapy technology
- What is Radiotherapy
- بررسی خطرات موجود در حین رادیوتراپی سازمان بهداشت جهانی
خطای یادکرد: خطای یادکرد: برچسب <ref> برای گروهی به نام «پانویس» وجود دارد، اما برچسب <references group="پانویس"/> متناظر پیدا نشد. ().