کربن آمورف
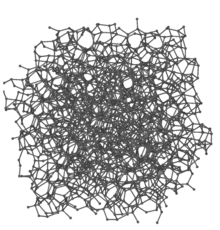
کربن آمورف یا کربن بیریخت، کربنی آزاد و واکنشی است که هیچ ساختار بلورینگی در آن دیده نمیشود. مواد کربن آمورف ممکن است با پایان دادن به پیوندهای معلق-π با هیدروژن تثبیت شوند. مانند سایر جامدات آمورف، میتوان نظم کوتاه بردی را مشاهده کرد. کربن آمورف در حالت کلی با نام aC و کربن آمورف هیدروژنی به شکل aC:H یا HAC و کربن آمورف هرمی با ta-C نمایش داده میشود. (کربن الماس مانند نیز نامیده میشود).[۱]
در کانیشناسی
ویرایشدر کانیشناسی، کربن آمورف نامی است که برای زغال سنگ، کربن مشتق شده از کاربید و سایر اشکال ناخالص کربن که نه گرافیت هستند و نه الماس استفاده میشود. با این حال، در مفهوم بلورنگاری، مواد واقعاً آمورف نیستند، بلکه مواد پلی کریستالی از گرافیت یا الماس[۲] در یک ماتریس کربن آمورف هستند. کربن تجاری نیز معمولاً حاوی مقادیر قابل توجهی از عناصر دیگر است که ممکن است ناخالصیهای کریستالی را نیز تشکیل دهند.
در علم مدرن
ویرایشبا توسعه تکنیکهای رسوبگذاری و رشد لایه نازک مدرن در نیمه دوم قرن بیستم، مانند انباشت بخار شیمیایی، رسوب پاششی و رسوبگذاری قوس یونی، ساخت مواد کربنی آمورف ممکن شد.
کربن آمورف دارای الکترونهای π موضعی است (برخلاف پیوندهای π آروماتیک در گرافیت)، و پیوندهای آن با طولها و فواصل متفاوت با سایر آلوتروپهای کربن تشکیل میشوند. همچنین حاوی غلظت بالایی از پیوندهای معلق است. اینها باعث انحراف در فاصله بین اتمی (که با استفاده از پراش اندازهگیری میشود) بیش از ۵٪ و همچنین تغییر قابل توجهی در زاویه پیوند ایجاد میکنند.[۲]
خواص لایههای کربن آمورف بسته به پارامترهای مورد استفاده در طی رسوب گذاری، متفاوت است. روش اولیه برای مشخص کردن کربن آمورف از طریق نسبت پیوندهای هیبرید شده sp2 به sp3 موجود در ماده است. گرافیت فقط از پیوندهای هیبرید شده sp2 تشکیل شدهاست، در حالی که الماس فقط از پیوندهای هیبرید شده sp3 تشکیل شدهاست. موادی که دارای پیوندهای هیبرید شده sp3 هستند، به دلیل شکل چهاروجهی تشکیل شده توسط پیوندهای هیبرید شده sp3، کربن آمورف چهار وجهی یا کربن الماس مانند (به دلیل شباهت بسیاری از خواص فیزیکی به الماس) نامیده میشوند.
بهطور تجربی، نسبتهای sp2 به sp3 را میتوان با مقایسه شدت نسبی پیکهای طیفسنجی مختلف (از جمله EELS، XPS وطیفسنجی رامان) با موارد مورد انتظار برای گرافیت یا الماس تعیین کرد. در کارهای نظری، نسبت sp2 به sp3 اغلب با شمارش تعداد اتمهای کربن با سه همسایه پیوندی در مقابل اتمهای با چهار همسایه پیوندی به دست میآید. (این تکنیک مستلزم تصمیمگیری بر روی یک متریک تا حدودی دلخواه برای تعیین اینکه آیا اتمهای همسایه پیوند خورده در نظر گرفته میشوند یا نه، و بنابراین صرفاً به عنوان نشانه ای از نسبت نسبی sp2-sp3 استفاده میشود)
اگرچه ممکن است به نظر برسد که مشخص کردن مواد کربن آمورف با نسبت sp2-sp3 نشاندهنده طیف یک بعدی از خواص بین گرافیت و الماس است، اما قطعاً اینطور نیست. تحقیقات در حال حاضر در مورد روشهایی برای توصیف و گسترش دامنه خواص ارائه شده توسط مواد کربن آمورف ادامه دارد.
تمام اشکال عملی هیدروکربن (مانند دود، دوده دودکش، زغال سنگ استخراج شده مانند قیر و آنتراسیت) حاوی مقادیر زیادی تار هیدروکربنی آروماتیک چند حلقه ای هستند و بنابراین تقریباً سرطان زا هستند.
کیو-کربن
ویرایشکیو-کربن (به انگلیسی:Q-carbon)، مخفف کربن خاموش شده، ادعا میشود که نوعی کربن آمورف است که فرومغناطیس، رسانای الکتریکی، سختتر از الماس[۳] و قادر به نمایش ابررسانایی در دمای بالا است.[۴] یک گروه تحقیقاتی به سرپرستی پروفسور جاگدیش نارایان و دانشجوی فارغالتحصیل آناگ باومیک در دانشگاه ایالتی کارولینای شمالی، کشف کیو کربن را در سال ۲۰۱۵ اعلام کردند.[۵]آنها مقالات متعددی در مورد سنتز و خصوصیات کیو-کربن منتشر کردهاند،[۶] اما تا اواخر سال ۲۰۲۰، هیچ تأیید تجربی مستقلی در مورد این ماده و خواص آن وجود ندارد.
به گفته محققان، کیو-کربن ساختار آمورف تصادفی را نشان میدهد که ترکیبی از پیوند ۳ طرفه (sp2) و ۴ طرفه (sp3) است، به جای پیوند یکنواخت sp3 موجود در الماس.[۷] کربن با استفاده از پالسهای لیزر نانوثانیه ذوب میشود، سپس به سرعت خاموش میشود تا کیو-کربن یا مخلوطی از کیو-کربن و الماس ایجاد شود. کیو-کربن را میتوان به شکلهای مختلفی ساخت، از نانوسوزن گرفته تا صفحات الماس بزرگ. محققان همچنین ایجاد نانوالماسهای خالی نیتروژن[۸] و کیو-نیترید بور (Q-BN)، و همچنین تبدیل کربن به الماس و h-BN به c-BN[۹] را در دمای محیط و هوا گزارش کردند. فشارها.[۱۰] این گروه حق ثبت اختراعات مربوط به مواد q را به دست آورد و قصد داشت آنها را تجاری کند.[۱۱]
در سال ۲۰۱۸، تیمی در دانشگاه تگزاس در آستین از شبیهسازیها برای ارائه توضیحات نظری در مورد خواص گزارششده کیو-کربن، از جمله رکورد ابررسانایی در دمای بالا، فرومغناطیس و سختی استفاده کردند.[۱۲][۱۳]با این حال، شبیهسازی آنها توسط سایر محققان تأیید نشدهاست.
جستارهای وابسته
ویرایشمنابع
ویرایش- ↑ Robertson, J. (1986). "Amorphous carbon". Advances in Physics. 35 (4): 317–374. Bibcode:1986AdPhy..35..317R. doi:10.1080/00018738600101911.
- ↑ ۲٫۰ ۲٫۱ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "diamond-like carbon films".
- ↑ Narayan, Jagdish; Gupta, Siddharth; Bhaumik, Anagh; Sachan, Ritesh; Cellini, Filippo; Riedo, Elisa (2018). "Q-carbon harder than diamond". MRS Communications (به انگلیسی). 8 (2): 428–436. doi:10.1557/mrc.2018.35. ISSN 2159-6859.
- ↑ Bromwich, Jonah (2015-12-03). "New Substance Is Harder Than Diamond, Scientists Say". The New York Times. ISSN 0362-4331. Retrieved Sep 22, 2019.
- ↑ Narayan, Jagdish; Bhaumik, Anagh (2015-12-07). "Novel phase of carbon, ferromagnetism, and conversion into diamond". Journal of Applied Physics. 118 (21): 215303. Bibcode:2015JAP...118u5303N. doi:10.1063/1.4936595. ISSN 0021-8979.
- ↑ "Researchers find new phase of carbon, make diamond at room temperature". Retrieved Sep 22, 2019.
- ↑ "Q-carbon is harder than diamond, incredibly simple to make | ExtremeTech". ExtremeTech. Retrieved Sep 22, 2019.
- ↑ Narayan, Jagdish; Bhaumik, Anagh (2016-11-02). "Novel synthesis and properties of pure and NV-doped nanodiamonds and other nanostructures". Materials Research Letters (به انگلیسی). 5 (4): 242–250. doi:10.1080/21663831.2016.1249805. ISSN 2166-3831.
- ↑ Narayan, Jagdish; Bhaumik, Anagh (February 2016). "Research Update: Direct conversion of h-BN into pure c-BN at ambient temperatures and pressures in air". APL Materials (به انگلیسی). 4 (2): 020701. doi:10.1063/1.4941095. ISSN 2166-532X.
- ↑ Narayan, Jagdish; Bhaumik, Anagh; Gupta, Siddharth; Haque, Ariful; Sachan, Ritesh (2018-04-06). "Progress in Q-carbon and related materials with extraordinary properties". Materials Research Letters (به انگلیسی). 6 (7): 353–364. doi:10.1080/21663831.2018.1458753. ISSN 2166-3831.
- ↑ Gupta, Siddharth; Sachan, Ritesh; Bhaumik, Anagh; Pant, Punam; Narayan, Jagdish (June 2018). "Undercooling driven growth of Q-carbon, diamond, and graphite". MRS Communications (به انگلیسی). 8 (2): 533–540. doi:10.1557/mrc.2018.76. ISSN 2159-6859.
- ↑ Sakai, Yuki; Chelikowsky, James R.; Cohen, Marvin L. (2018-02-01). "Simulating the effect of boron doping in superconducting carbon". Physical Review B. 97 (5): 054501. arXiv:1709.07125. Bibcode:2018PhRvB..97e4501S. doi:10.1103/PhysRevB.97.054501.
- ↑ Sakai, Yuki; Chelikowsky, James R.; Cohen, Marvin L. (2018-07-13). "Magnetism in amorphous carbon". Physical Review Materials. 2 (7): 074403. arXiv:1803.11336. doi:10.1103/PhysRevMaterials.2.074403.