کاربید تانتالوم
تانتال کاربید (به انگلیسی: Tantalum carbide) یا کاربید تانتالوم با فرمول شیمیایی TaCx یک ترکیب شیمیایی است. کاربیدهای تانتال، خانوادهای دوتایی از تانتال و کربن را با فرمول تجربی TaCx تشکیل میدهند که معمولا x بین 0.4 تا 1 متغیر است.این مواد به شدت سخت، ترد و مواد سرامیکی دیرگداز با رسانایی الکتریکی هستند. شکل ظاهری این ترکیب به صورت پودر قهوهای-خاکستری بیبو است که معمولا توسط زینترینگ فرآوری میشوند.[۱]
نقطه ذوب کاربید های تانتالوم 3880 درجه سانتی گراد (بیشترین مقدار) بسته به خلوص و شرایط اندازه گیری است، این مقدار میان بالاترینها برای ترکیبات دوتایی است.[۲][۳]
این ماده دیرگداز و بهبود دهنده نقشی مهم را در کاربیدهای سرامیکی بازی میکند.
| Tantalum carbide | |
|---|---|
| |

| |
Tantalum carbide | |
دیگر نامها Tantalum(IV) carbide | |
| شناساگرها | |
| شماره ثبت سیایاس | 12070-06-3 |
| جیمول-تصاویر سه بعدی | Image 1 |
| |
| |
| خصوصیات | |
| فرمول مولکولی | TaC |
| جرم مولی | 192.96 g/mol |
| شکل ظاهری | Brown-gray powder |
| بوی | Odorless |
| چگالی | 14.3–14.65 g/cm3 (TaC) 15.1 g/cm3 (TaC0.5)[۴] |
| دمای ذوب | ۳٬۸۵۰–۳٬۸۸۰ درجه سلسیوس (۶٬۹۶۰–۷٬۰۲۰ درجه فارنهایت؛ ۴٬۱۲۰–۴٬۱۵۰ کلوین) (TaC)[۵] ۳٬۳۲۷ درجه سلسیوس (۶٬۰۲۱ درجه فارنهایت؛ ۳٬۶۰۰ کلوین) (TaC0.5)[۴] |
| دمای جوش | ۴٬۷۸۰–۵٬۴۷۰ درجه سلسیوس (۸٬۶۴۰–۹٬۸۸۰ درجه فارنهایت؛ ۵٬۰۵۰–۵٬۷۴۰ کلوین) (TaC)[۴][۵] |
| انحلالپذیری در آب | Insoluble |
| انحلالپذیری | Soluble in HF-HNO3 mixture[۴] |
| رسانندگی گرمایی | 21 W/m·K[۵] |
| ترموشیمی | |
| 36.71 J/mol·K[۶] | |
آنتروپی مولار
استاندارد S |
42.29 J/mol·K |
آنتالپی استاندارد
تشکیل ΔfH |
-144.1 kJ/mol |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
خواص آلیاژها را به وسیلهی بهتر کردن ساختار فیبری و استحاله فازی سینتیکی، افزایش استحکام آلیاژ،پایدار کردن فاز و قابلیت فرآوری آن بهبود میبخشد.
این تانتال کاربیدها ممکن است نقطه ذوبی کمی بالاتر در حدود 3942 درجه سانتیگراد داشته باشند.[۷]
کاربرد ها
ویرایش1.دیرگداز فوق دمای بالاست که کاربرد های دیرگدازی مختلفی از خود نشان میدهد.در دسته سرامیک های فوق دمای بالا (UHTC) قرار میگیرد.
2. معمولاً به کاربید تنگستن و کبالت در حین فرآیند سایش مکانیکی اضافه میشود تا خواص فیزیکی ساختار زینتر را بهبود ببخشد. همچنین نقش ممانعت کننده در مقابل رشد دانه برای جلوگیری از تشکیل دانه های بزرگ را بازی می کند از این رو باعث تولید ماده با سختی بهینه می شود.
3. به عنوان پوششی برای قالب های فولادی در فرایند قالب تزریقی آلیاژهای آلومینیوم استفاده می شود.
4. تانتال کاربید در تولید ابزار تیز با مقاومت مکانیکی و سختی فوقالعاده و برای تیغههای برش در ابزار برش استفاده میشود.
5. در سیستم حفاظت حرارتی در وسایل نقلیه با سرعت بالا یا صنایع هوافضا و به عنوان محفظه سوخت در محیطهای فوق حرارتی در راکتورهای هسته ای استفاده می شود.
6. از موارد دیگر به تسلیحات ضدگلوله، باتریها، اجزای الکترونیکی و تجهیزات شیمیایی میتوان اشاره کرد.
7. افزودن تانتال کاربید به مواد کامپوزیتی کربن کربن منجر به کاهش شرایط انبساط حرارتی شده و باعث افزایش مقاومت به اکسیداسیون و مقاومت سایشی فلزات دیرگداز میشود.
آماده سازی
ویرایشپودرها و ویسکرهای کاربید تانتالوم به روشهای احیای کربوترمال، پلاسمای حرارتی، سل ژل، حرارت مایکروویو، احیای آلکالی، سنتز دمای بالای خود تکثیری (SHS) و زینتر حرارتی القایی فرکانس بالا تولید میشوند.[۸]
در یکی از این روش ها پودرهای TaCx ترکیبات مطلوب به وسیله حرارت دهی یک مخلوط پودرهای تانتالوم و گرافیت در خلاء یا اتمسفر گاز خنثی (آرگون) ساخته می شوند.این حرارت در یک دمای حدود 2000 با استفاده از کوره یا یک سیستم ذوب قوس ایجاد می شود.[۹][۱۰]یک روش متداول فرآیند احیاء (Reduction) تانتالوم پنتوکسید به وسیله کربن در اتمسفر خلاء یا هیدروژن در دمای 1500 تا 1700 است. این روش برای مشاهده تانتال کاربید در 1876 استفاده می شد اما کمبودهای آن استوکیومتری محصول را کنترل می کند. [۱۱]
تولید TaC به طور مستقیم از عناصر به صورت عدد تکثیری (self propagation) در میان سنتز دمای بالا گزارش شده است.[۱۲]
ساختمان کریستالی
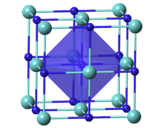
ویرایشترکیبات TaCx یک ساختار کریستالی مکعبی (سنگ نمک) برای X= 0.7 _ 1.0 دارند.[۱۳] پارامتر شبکه با X افزایش پیدا میکند.[۱۴]
ماده TaC0.5 دو شکل کریستالی اصلی دارد. گونه پایدارتر آن یک ساختار تریگونال از نوع آنتی یدید کادمیوم است که در دمای بالای ۲۰۰۰ درجه سانتیگراد به هگزاگونال و بدون نظم بلند دامنه برای اتم های کربن، تغییر شکل می دهد.[۹]
| فرمول | ساختار | نوع | نماد پیرسون | Space group | شماره | Z | چگالی (g/cm3) | (a (nm | (c (nm |
|---|---|---|---|---|---|---|---|---|---|
| TaC | Cubic | NaCl[۱۵] | cF8 | Fm۳m | 225 | 4 | 14.6 | 0.4427 | |
| TaC0.75 | Trigonal[۱۶] | hR24 | R۳m | 166 | 12 | 15.01 | 0.3116 | 3 | |
| TaC0.5 | Trigonal[۱۷] | anti-CdI2 | hP3 | P۳m1 | 164 | 1 | 15.08 | 0.3103 | 0.4938 |
| TaC0.5 | Hexagonal[۱۸] | hP4 | P63/mmc | 194 | 2 | 15.03 | 0.3105 | 0.4935 |
(در جدول ) Z تعداد واحدهای فرمول بر هر سلول واحد است. چگالی محاسبه شده از پارامتر شبکه است.
خواص
ویرایشپیوند بین اتمهای تانتالوم و کربن در تانتال کاربید یک مخلوط پیچیده از تلفیق یونی، فلزی و کوالانت است و به خاطر جزء کووالانت قوی این کاربیدها موادی بسیار سخت و ترد هستند.برای مثال، TaC میکروسختی 1600 _ 2000 kg/mm² [۱۹] معادل با 9 mohs (فقط الماس از آن سخت تر است) و مدول الاستیک 285 GPa دارد ، در جایی که این مقادیر برای خود تانتالوم 110 kg/mm² و 186 GPa است.[۲۰]
سختی، تنش تسلیم و تنش برشی با مقدار کربن در TaCx افزایش می یابد. کاربردهای تانتالوم رسانایی الکتریکی فلزی دارند که هر دوی آنها به بزرگی مقدار و دما بستگی دارند. TaC یک ابر رسانا با دمای انتقال نسبتاً بالای Tc=10.35 K است.[۱۴]
بیشترین مقاومت دیرگدازی برای تانتال کاربید است.
تنها مادهای است که خواص مکانیکی مشخصی را در دمای ۲۹۰۰ درجه سانتیگراد تا ۳۲۰۰ درجه سانتی گراد نگه می دارد و باقی می ماند، با این وجود نقص آن حساسیت زیاد به شوک حرارتی، رسانایی حرارتی پایین و ضریب انبساط حرارتی بالای آن است که باعث محدود شدن در استفاده های هوا فضا شده است.
منابع
ویرایش- ↑ Emsley, John (11 August 2003). Nature's building blocks: an A-Z guide to the elements. Oxford University Press. pp. 421–. ISBN 978-0-19-850340-8. Retrieved 2 May 2011
- ↑ The claim of melting point of 4000 °C in TaC0.89 is based not on actual measurement but on an extrapolation of the phase diagram, using an analogy with NbC, see Emeléus
- ↑ Emeléus, Harry (1968). Advances in Inorganic Chemistry and Radiochemistry. Academic Press. pp. 174–176. ISBN 978-0-12-023611-4. Retrieved 3 May 2011
- ↑ ۴٫۰ ۴٫۱ ۴٫۲ ۴٫۳ Lide, David R., ed. (2009). هندبوک شیمی و فیزیک سیآرسی (90th ed.). بوکا راتون، فلوریدا: انتشارات سیآرسی. ISBN 978-1-4200-9084-0.
- ↑ ۵٫۰ ۵٫۱ ۵٫۲ 5196273
- ↑ Tantalum carbide in Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (retrieved 2014-07-02)
- ↑ Agte, C.; Alterthum, H. (1930). "Researches on Systems with Carbides at High Melting Point and Contributions to the Problem of Carbon Fusion". Zeitschrift für technische Physik. 11: 182–191. ISSN 0373-0093.
- ↑ «نسخه آرشیو شده». بایگانیشده از اصلی در ۱۹ ژانویه ۲۰۲۰. دریافتشده در ۲۲ مارس ۲۰۲۰.
- ↑ ۹٫۰ ۹٫۱ Lonnberg, B; Lundstrom, T; Tellgren, R (1986). "A neutron powder diffraction study of Ta2C and W2C". Journal of the Less Common Metals. 120 (2): 239–245. doi:10.1016/0022-5088(86)90648-X
- ↑ Rudy, Erwin; Brukl, C. E.; Windisch, Stephan (1968). "Constitution of Ternary Ta-Mo-C Alloys". Journal of the American Ceramic Society. 51 (5): 239–250. doi:10.1111/j.1151-2916.1968.tb13850.x.
- ↑ Joly, A. (1876). "Sur les azotures et carbures de niobium et de tantale". Compt. Rend.(in French). 82: 1195
- ↑ Shuck, Christopher E.; Manukyan, Khachatur V.; Rouvimov, Sergei; Rogachev, Alexander S.; Mukasyan, Alexander S. (January 2016). "Solid-flame: Experimental validation". Combustion and Flame. 163: 487–493. doi:10.1016/j.combustflame.2015.10.025.
- ↑ Lavrentyev, A; Gabrelian, B; Vorzhev, V; Nikiforov, I; Khyzhun, O; Rehr, J (2008). "Electronic structure of cubic HfxTa1–xCy carbides from X-ray spectroscopy studies and cluster self-consistent calculations". Journal of Alloys and Compounds. 462 (1–2): 4–10. doi:10.1016/j.jallcom.2007.08.01
- ↑ ۱۴٫۰ ۱۴٫۱ Valvoda, V. (1981). "X-ray diffraction study of Debye temperature and charge distribution in tantalum monocarbide". Physica Status Solidi A. 64: 133–142. doi:10.1002/pssa.2210640114
- ↑ Valvoda, V. (1981). "X-ray diffraction study of Debye temperature and charge distribution in tantalum monocarbide". Physica Status Solidi A. 64: 133–142. doi:10.1002/pssa.2210640114.
- ↑ Yvon, K.; Parthé, E. (1970). "On the crystal chemistry of the close-packed transition-metal carbides. I. The crystal structure of the [zeta]-V, Nb and Ta carbides". Acta Crystallographica Section B. 26 (2): 149–153. doi:10.1107/S0567740870002091.
- ↑ Bowman, A. L.; Wallace, T. C.; Yarnell, J. L.; Wenzel, R. G.; Storms, E. K. (1965). "The crystal structures of V2C and Ta2C". Acta Crystallographica. 19: 6–9. doi:10.1107/S0365110X65002670.
- ↑ Rudy, Erwin; Brukl, C. E.; Windisch, Stephan (1968). "Constitution of Ternary Ta-Mo-C Alloys". Journal of the American Ceramic Society. 51 (5): 239–250. doi:10.1111/j.1151-2916.1968.tb13850.x.
- ↑ Kurt H. Stern (1996). Metallurgical and Ceramic Protective Coatings. Chapman & Hall.
- ↑ «The chemistry of transition metal carbides and nitrides».
- «IUPAC GOLD BOOK». دریافتشده در ۱۸ مارس ۲۰۱۲.