مغز انسان
مغز انسان، عضو مرکزی دستگاه عصبی انسان است که به همراه طناب نخاعی، دستگاه عصبی مرکزی را تشکیل میدهند. مغز، شامل مخ، ساقه مغز و مخچه است. این عضو، اکثر فعالیتهای بدن، همچون پردازش، یکپارچه سازی و هماهنگکردن اطلاعات دریافتی از اعضای حسی را کنترل کرده و با ارسال دستورالعملهایی به سایر نقاط بدن، تصمیمسازی میکند. مغز در استخوانهای جمجمه قرار داشته و توسط آنها محافظت میشود.
| مغز انسان | |
|---|---|
 مغز انسان و جمجمه | |
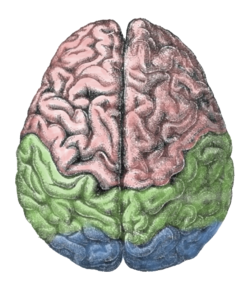 لوبهای بالایی از نیمکرههای مخ: لوبهای پیشانی (صورتی)، لوبهای آهیانهای (سبز)، لوبهای پسسری (آبی) | |
| جزئیات | |
| ساخته از | لوله عصبی |
| دستگاه | دستگاه عصبی مرکزی |
| سرخرگها | سرخرگ کاروتید درونی، سرخرگ مهرهای |
| سیاهرگها | سیاهرگ ژوگولار داخلی، وریدهای داخلی مخ؛ وریدهای خارجی: (فوقانی، میانی و وریدهای مخ تحتانی)، ورید قاعدهای و وریدهای مخچهای |
| شناسهها | |
| لاتین | Cerebrum[۱] |
| یونانی | ἐγκέφαλος (enképhalos)[۲] |
| TA98 | A14.1.03.001 |
| TA2 | 5415 |
| FMA | 50801 |
مخ، بزرگترین بخش از مغز انسان بوده و شامل دو نیمکره است. هستهٔ داخلی هر نیمکره از ماده سفید و سطح خارجی — قشر مغز — از ماده خاکستری تشکیل شدهاست. قشر مغز دارای لایهای خارجی به نام نئوکورتکس و لایهای داخلی به نام آلوکورتکس[الف] است. نئوکورتکس از شِش لایه نورونی تشکیل شده در حالی که آلوکورتکس، سه یا چهار لایه نورونی دارد. هر نیمکره بهطور قراردادی به چهار لوب پیشانی، گیجگاهی، آهیانه، پسسر تقسیم شده که به وسیله چین خوردگیهای عمیقی از یکدیگر جدا شدهاند. لوب پیشانی، جایگاه عملکردهای اجرایی همچون خود-کنترلی، برنامهریزی، استدلال و تفکر مجرد است در حالی که لوب پسسری به بینایی اختصاص داده شدهاست. در داخل هر لوب، نواحی قشری دارای مناطق عملکردی بهخصوصی چون حسی، حرکتی و ارتباطی[ب] است. گرچه نیمکرههای چپ و راست شباهت گستردهای از نظر شکل و عملکرد با یکدیگر دارند، اما برخی از این عملکردها مرتبط با یک سمت اند، همچون زبان که به نیمکره چپ و توانایی تصور بصری-فضایی که به نیمکره راست مغز مرتبط اند. نیمکرهها توسط نوارهای عصبی رابط به هم متصل میشوند، بزرگترین این نوارها، جسم پینهای است.
مخ، توسط ساقه مغز به طناب نخاعی متصل شده که خود دارای سه بخش میانمغز، پل مغز و بصل النخاع است. مخچه توسط سه جفت نوار عصبی به نام پایکهای مخچهای[پ] به ساقه مغز متصل میشود. در مخ، دستگاه بطنی شامل چهار بطن به هم متصل، قرار دارد که در آنها مایع مغزی-نخاعی تولید شده و به گردش در میآید. زیرِ قشر مخ، ساختارهای مهم و متعددی مانند تالاموس، اپیتالاموس، غده پینهآل، هیپوتالاموس، غده هیپوفیز، سابتالاموس، ساختارهای لیمبیک (شامل آمیگدال و هیپوکامپ)، کلاستروم[ت]، هستههای مختلف از عقدههای قاعدهای (شامل ساختارهای قاعدهای مغز قدامی و سه عضو دور بطنی[ث]) قرار دارد. سلولهای مغز شامل نورونها و سلولهای گلیال پشتیبان هستند. بیش از ۸۶ میلیارد نورون در مغز وجود دارند و تعداد سایر سلولهای مغز نیز عددی کم و بیش برابر با همین مقدار است. فعالیت مغزی به دلیل اتصالات بین نورونی و آزاد شدن ناقلان عصبی از آنها، در پاسخ به پتانسیل عمل شکل میگیرد. نورونها به یکدیگر متصل میشوند تا مسیرهای نورونی، مدارهای عصبی و سامانههای شبکهای را تشکیل دهند؛ نتیجه این ساختار، مداری است که براساس فرایند انتقال عصبی[ج] عمل میکند.
مغز دارای سه فرایند محافظتی به نامهای جمجمه، مایع مغزی-نخاعی و سد خونی-مغزی است. جمجمه، مغز را از آسیبهای احتمالی حفظ میکند، مایع مغزی-نخاعی، مغز را در استخوان جمجمه ثابت نگه میدارد و سد خونی-مغزی دارای مویرگهای پیوسته بوده و مغز را از جریان عمومی خون جدا میکند. با این حال، مغز هنوز هم در معرض آسیب، بیماری و عفونت قرار دارد. آسیب ممکن است توسط تروما یا فقدان تغذیه خونی ناشی از سکته باشد. مغز نسبت به اختلالات زوال آسیبپذیر است، این اختلالات شامل بیماری آلزایمر، MS و HAND میشود. تصور بر این است که بسیاری از بیماریهای روانی مانند اسکیزوفرنی و افسردگی بالینی با بدعملکردیهای مغزی مرتبط باشد. همچنین ممکن است مغز، محل تومورهای خوشخیم و بدخیم شود که عمدهٔ این تومورها از متاستاز سایر نقاط بدن ایجاد میگردد.
مطالعه کالبدشناسی مغز را نوروآناتومی و مطالعه عملکردهای مغزی را علوم اعصاب مینامند. فنون مختلفی جهت مطالعه مغز به کار میروند. بهطور سنتی، ساختار مغزی دیگر جانوران بررسی و مطالعات میکروسکوپی بر روی آنها صورت میگیرد. این روش بررسی غالباً بر روی جانورانی با ساختاری نزدیک به انسان مانند انسانسانان انجام و با فرایندهای مشابه در انسان مقایسه میشود. همچنین فناوریهای تصویربرداری پزشکی چون تصویربرداری عصبی کارکردی و نوار مغزی (EEG) در مطالعه مغز نقش مهمی را ایفا میکنند. تاریخچه پزشکی افراد دچار آسیب مغزی، باعث شدهاست که بینش ما نسبت به عملکرد هر بخش از مغز افزایش یابد. تحقیقات روی مغز طی زمان پیشرفت کرده و مراحلِ فلسفی، آزمایشی و نظری را پشت سر نهادهاست. یکی از این مراحل نوظهور، شبیهسازی فعالیتهای مغزی است.[۳]
فلسفه ذهن برای قرنها تلاش کرده تا مسئلهٔ طبیعتِ خودآگاهی و مسئلهٔ ذهن و بدن[چ] را حل کند. شبهعلمی به نام فرنولوژی تلاش کرد تا در قرن نوزدهم میلادی، ویژگیهای شخصیتی را در نواحی از قشر مغزی موضعسازی کند. در داستانهای علمی-تخیلی، پیوند مغز در قالب افسانههایی چون مغزِ دونووان (۱۹۴۲ میلادی)[ح] به تصویر کشیده شدهاست.
ساختار ویرایش
ماکروآناتومی ویرایش
مغز انسان بالغ بهطور میانگین وزنی بین ۱٫۲ تا ۱٫۴ کیلوگرم دارد که در حدود ۲ درصد از وزن کل بدن است.[۴][۵] حجم مغز در مردان حدود ۱۲۶۰ و در زنان ۱۱۳۰ سانتیمتر مکعب است.[۶] وزن مغز بین افراد مختلف دارای نوسان زیادی است،[۶] به طوری که رنج مرجع استاندارد برای مردان ۱٬۱۸۰ تا ۱٬۶۲۰ گرم[۷] و برای زنان ۱٬۰۳۰ تا ۱٬۴۰۰ گرم است.[۸]
مخ، شامل نیمکرههای مغز است که بزرگترین بخش مغز را تشکیل داده و بر روی سایر ساختارهای مغزی قرار دارد.[۹] ناحیه بیرونی نیمکرهها، یعنی قشر مغز (ماده خاکستری)، شامل لایههای قشری از نورونها است. هر نیمکره به وسیله شیارهایی به چهار لوب تقسیم میگردد: لوب پیشانی، لوب آهیانهای، لوب گیجگاهی و لوب پسسری.[۱۰] برخی منابع سه لوب دیگر را نیز فهرست میکنند که شامل یک لوب مرکزی، لوب لیمبیک و لوب اینسولار است.[۱۱] لوب مرکزی، شکنج پیشمرکزی[د] و شکنج پسمرکزی[ذ] را تشکیل میدهد و آن را به عنوان لوبی مجزا در نظر گرفتهاند، چرا که نقش عملکردی متمایزی دارد.[۱۱][۱۲]
ساقه مغز که شبیه ساقه است، در ابتدای ناحیه میانمغز به مخ متصل شده و در همان موقعیت از مخ خارج میشود. ساقه مغز شامل میانمغز، پل مغز و بصل النخاع است. پشت ساقه مغز، مخچه[ر] قرار دارد.[۹]
مخ، ساقه مغز، مخچه و طناب نخاعی توسط سه لایه مننژ پوشیده شدهاند. این سه لایه از خارج به داخل شامل لایهٔ سختی به نام سختشامه، لایهٔ میانیِ عنکبوتیه و لایه لطیف نرمشامه (لایه ای که در تماس با مغز است) هستند. بین عنکبوتیه و نرمشامه، فضای زیرعنکبوتیه و تیغههای زیرعنکبوتیهای قرار دارد که شامل مایع مغزی-نخاعی میشود.[۱۳] بیرونیترین غشای قشر مخ، غشای قاعدهای نرمشامه به نام گلیای محدود کننده[ز] قرار داشته که بخش مهمی از سد خونی-مغزی است.[۱۴] مغز زنده بسیار نرم بوده و مثل توفو حالتی ژل مانند دارد.[۱۵] لایههای قشری از جنس نورون، بخش اعظم ماده خاکستری مخ را تشکیل میدهند، در حالی که نواحی زیرقشری از جنس آکسونهای میلینی شده، ماده سفید را تشکیل میدهند.[۹] مادهٔ سفید مغز، حدود نیمی از حجم کلِ مغز را شامل میشود.[۱۶]
مخ ویرایش
مخ، بزرگترین بخش مغز است و توسط شکاف عمیقی به نام شیار طویلی،[ژ] به نیمکرههای چپ و راست تقسیمبندی میشود که تقریباً متقارن اند.[۱۷] به عدم تقارن بین لوبها، پتالیا[س] میگویند.[۱۸] نیمکرهها توسط پنج رابط به هم متصل اند که کل شیار طولی را پیموده و بزرگترین بخش آن را جسم پینهای مینامند.[۹] هر نیمکره به صورت قراردادی به چهار لوب اصلی تقسیمبندی میگردند؛ لوب پیشانی، لوب آهیانهای، لوب گیجگاهی و لوب پسسری که نامگذاریشان براساس استخوانهای جمجمهای است که بر روی هر کدام از این قسمتها قرار دارند.[۱۰] هر لوب با یک یا دو عملکرد اختصاصی همراه است که این عملکردها با یکدیگر همپوشانی دارند.[۱۹] سطح مغز چین خوردگیهایی دارد که به برآمدگیهایی به نام شکنج[ش] و فرورفتگیهایی به نام شیار[ص] تقسیمبندی شده و اغلب براساس موقعیتشان نامگذاری میشوند، همچون شکنج پیشانی از لوب پیشانی یا شیار مرکزی که نواحی مرکزی نیمکرهها را از هم جداسازی میکند. تغییرات کوچک بسیاری در نوع چین خوردگیهای دوم و سوم افراد مختلف وجود دارد.[۲۰]
بخش بیرونی مخ را قشر مغز مینامند که از ماده خاکستری تشکیل شده و در لایههای مختلف آرایش یافتهاند. این لایه بین ۲ تا ۴ میلیمتر ضخامت دارد و به صورت عمیق تا خورده و ظاهری پیچخورده را ایجاد میکند.[۲۱] زیر قشر مغز، ماده سفید مخی قرار دارد. بزرگترین بخش از قشر مخ، نئوکورتکس است که دارای شش لایه نورونی است. باقی قشر را آلوکورتکس مینامند که دارای سه یا چهار لایه است.[۹]
با تقسیمبندی قشر به حدود پنجاه ناحیه عملکردی متفاوت به نام نواحی برادمن،[ض] بر روی قشر مغز نقشهای نگاشته شدهاست. وقتی این نواحی زیر میکروسکوپ دیدهشوند، تمایز واضحی بینشان دیده میشود.[۲۲] قشر به دو ناحیه عملکردی اصلی تقسیم میشود: یک قشر حرکتی و یک قشر حسی.[۲۳] قشر حرکتی اولیه که آکسونها را به سمت پایینِ نورونهای حرکتی در ساقه مغز و طناب نخاعی میفرستد، بخش عقبی لوب پیشانی را در جلوی ناحیه پیکری-حسی اشغال میکند. نواحی حسی اولیه، پیامها را از طریق هستههای رلهای از اعصاب حسی و نوارها در تالاموس دریافت میکنند. نواحی حسی اولیه شامل قشر بصری لوب پسسری، قشر شنوایی در بخشهایی از لوب گیجگاهی، قشر اینسولار و قشر پیکری-حسی در لوب آهیانهای است. بخشهای باقیمانده از قشر را نواحی ارتباطی[ط] مینامند. این نواحی ورودیهایشان را از نواحی حسی و بخشهای پایینتر مغز دریافت کرده و درگیر فرایندهای شناختی پیچیدهٔ ادراک، تفکر و تصمیمگیری اند.[۲۴] عملکردهای اصلی لوب پیشانی مربوط به کنترل توجه، تفکر انتزاعی، رفتار، حل مسئله و واکنشهای فیزیکی و شخصیت است.[۲۵][۲۶] لوب پسسری، کوچکترین لوب بوده و عملکردهای اصلی آن شامل ادراک بصری، پردازش بصری-فضایی، حرکت و ادراک رنگ است.[۲۵][۲۶] یک لبول کوچکتر به نام کونئوس نیز در لوب پس سری وجود دارد که وظیفه پردازش اطلاعات اولیه بینایی را بر عهده دارد.[۲۷] این لبول در کنترل فرایندهای اختلال دو قطبی نیز بسیار حائز اهمیت است.[۲۷] لوب گیجگاهی خاطرات شنوایی، بصری، زبانی و برخی از خاطرات گفتاری را کنترل میکند.[۲۵]
مخ شامل بطنها است که مایع مغزی-نخاعی در آن مکانها تولید شده و به گردش در میآید. در زیر جسم پینهای، دیوارهٔ شفاف[ظ] قرار دارد که غشای جداکنندهٔ بطنهای طرفی میباشد. در زیر بطنهای طرفی، تالاموس و در جلو و پایین آن نیز هیپوتالاموس قرار دارد. هیپوتالاموس به جلو کشیده شده و غده هیپوفیز را شکل میدهد. عقبِ تالاموس، ساقهٔ مغز واقع شدهاست.[۲۸]
عقدههای قاعدهای که به آنها هستههای قاعدهای نیز گفته میشود، دستهای از ساختارها در عمق نیمکرهها هستند که درگیر تنظیم رفتار و حرکت میباشند.[۲۹] بزرگترین مؤلفهٔ آن، جسم مخطط است، سایر مؤلفهها گلوبوس پالیدوس، توده سیاه و هسته سابتالاموس هستند.[۲۹] جسم مخطط به بخش شکمی و پشتی دستهبندی میشود، تقسیمبندی که براساس عملکرد و ارتباطات بنا شدهاست. جسم مخطط شکمی شامل هسته اکومبنس[ع] و پیاز بویایی[غ] است در حالی که جسم مخطط پشتی شامل هسته دمدار و پوتامن است. پوتامن و گلوبوس پالیدوس توسط کپسول داخلی از بطنهای طرفی و تالاموس جدا شدهاند، در حالی که هسته دمدار حول بطنهای طرفی و روی وجوه بیرونی آن کشیده شده و بر آنها مماس است.[۳۰] در عمیقترین بخش شیار جانبی، بین قشر اینسولار و جسم مخطط، ورقه نورونی نازکی به نام کلاستروم قرار دارد.[۳۱]
در پایین و جلوی جسم مخطط، تعدادی از ساختارهای مغز قدامی قاعدهای[ف] قرار دارند. این ساختارها شامل این موارد اند: نوکلئوس باسالیس،[ق] نوار قطری بروکا،[ک] سابستنشا اینومیناتا[گ] و هسته سپتال مدیال. این ساختارها در تولید ناقل عصبی به نام استیلکولین مهم اند، که پس از تولید بهطور گسترده در سرتاسر مغز منتشر میگردد. مغز قدامی قاعدهای، به خصوص نوکلئوس باسالیس را به عنوان خروجی کولینرژیک اصلیِ دستگاه عصبی مرکزی به جسم مخطط و نئوکورتکس در نظر میگیرند.[۳۲]
مخچه ویرایش
مخچه به یک لوب قدامی، یک لوب خلفی و لوب فلوکولوندولار[ل][۳۳] تقسیمبندی میگردد. کرمینه، بین لوبهای خلفی و قدامی قرار داشته و آنها را به هم متصل میکند.[۳۴] مخچه، در مقایسه با قشر مخ، قشر بیرونی بسیار نازکتری دارد، به طوری که شیارهای باریکی بر روی آن چندین چین خوردگی عرضی خمیده را ایجاد میکنند.[۳۴] زیر و بین این دو لوب، لوب سوم فلوکولوندولار قرار دارد.[۳۵] مخچه در سمت عقب حفره کرانیال قرار دارد، به طوری که زیر لوبهای پسسری قرار داشته و توسط چادرینه مخچه که ورقهای از فیبرها است از اینها جدا شدهاست.[۳۶]
مخچه توسط سه جفت از نوارهای عصبی به نام پایکهای مخچهای[م] به ساقه مغز وصل شدهاند. جفت پایکهای فوقانی به میانمغز، جفت پایکهای میانی به بصل النخاع و جفت پایک تحتانی نیز به پل مغزی متصل میشوند.[۳۴] مخچه شامل بخشی از بصل النخاعِ داخلی از جنس ماده سفید و یک قشر خارجی از جنس ماده خاکستری که غنی از چینخوردگی است.[۳۶] به نظر میرسد که لوبهای قدامی و خلفی مخچه در هماهنگکردن و هموار سازی حرکات پیچیده و لوب فلوکولوندولار نیز در حفظ تعادل نقش ایفا میکند[۳۷] گرچه که اختلاف نظرهایی در مورد عملکردهای شناختی، رفتاری و حرکتی آن وجود دارد.[۳۸]
ساقه مغز ویرایش
ساقه مغز در زیر مخ قرار دارد و از میانمغز، پل مغز و مدولا تشکیل شدهاست. در قسمت پشتی جمجمه، حفره کرانیال قدامی و بر روی قسمتی از قاعده جمجمه معروف به کلیووس قرار دارد و به سوراخ بزرگ پسسری در استخوان پسسری ختم میشود. ساقه مغز در زیر آن به عنوان طناب نخاعی ادامه مییابد که توسط ستون مهره ای محافظت میشود.[۳۹]
ده جفت از دوازده جفت اعصاب مغزی مستقیماً از ساقه مغز خارج میشوند.[۳۹] ساقه مغز همچنین حاوی بسیاری از هستههای عصبی جمجمه و هستههای اعصاب محیطی و همچنین هستههایی است که در تنظیم بسیاری از فرآیندهای ضروری از جمله تنفس ، کنترل حرکات چشم و تعادل نقش دارند.[۴۰][۳۹] سازند مشبک، شبکهای از هستههایی با شکلگیری نامشخص، در داخل و در طول ساقه مغز وجود دارد.[۳۹] بسیاری از تنه عصبی، که اطلاعات را به و از قشر مغز به بقیه بدن منتقل میکنند، از ساقه مغز عبور میکنند.[۳۹]
میکروآناتومی ویرایش
مغز انسان اساساً از نورونها، سلولهای گلیال، سلولهای بنیادی عصبی[ن] و رگهای خونی تشکیل شدهاست. انواع نورون شامل نورونهای داخلی، سلولهای هرمی از جمله سلولهای بتز، نورونهای حرکتی (نورون حرکتی فوقانی و نورون حرکتی تحتانی) و مخچه سلولهای پورکنژ. سلولهای بتز بزرگترین سلولها (بر اساس اندازه بدن سلولی) در سیستم عصبی هستند.[۴۱] تخمین زده میشود که مغز انسان بالغ دارای ۸±۸۶ میلیارد نورون است که تعداد آنها تقریباً برابر (۱۰±۸۵ میلیارد) سلول غیر عصبی است.[۴۲] از این نورونها، ۱۶ میلیارد (۱۹٪) در قشر مغز و ۶۹ میلیارد (۸۰٪) در مخچه قرار دارند.[۴۲]
انواع سلولهای گلیال آستروسیتها (از جمله برگمان گلیا[و]، الیگودندروسیتها، سلولهای اپاندیمی (شامل تانیسیتها[ه]، سلولهای گلیال شعاعی، میکروگلیا و زیرگروهی از سلولهای پیش ساز الیگودندروسیت هستند. آستروسیتها بزرگترین سلولهای گلیال هستند. آنها سلولهای ستارهای[ی] هستند که فرآیندهای زیادی از جسم سلولی آنها تابش میشود. برخی از این فرایندها به صورت پاهای انتهایی اطراف عروقی بر روی دیوارههای مویرگ ختم میشوند. گلیا لیمیتانس[اا] قشر از فرآیندهای آستروسیتی پا تشکیل شدهاست که بخشی از سلولهای مغز را شامل میشود.
ماستسلها گلبولهای سفید خونی هستند که در سیستم عصبی ایمنی[اب] مغز تعامل دارند.[۴۳] ماست سلها در سیستم عصبی مرکزی در تعدادی ساختار از جمله مننژها وجود دارند.[۴۳] آنها به عنوان واسطه در واکنشهای عصبی ایمنی در شرایط التهابی حضور دارند و به حفظ سد خونی مغزی، بهویژه در مناطقی از مغز که مانع وجود ندارد، کمک میکنند.[۴۳][۴۰] ماست سلها همان عملکردهای کلی را در بدن و سیستم عصبی مرکزی مانند تأثیرگذاری یا تنظیم پاسخهای آلرژیک، ایمنی ذاتی و سازگار، خودایمنی و التهاب را انجام میدهند.[۴۳] ماست سلها به عنوان سلول مؤثر [اپ] اصلی عمل میکنند که از طریق آن پاتوژنها میتوانند سیگنالهای بیوشیمیایی را که بین دستگاه گوارش و سیستم عصبی مرکزی انجام میشود تحت تأثیر قرار دهند.[۴۴][۴۵]
نشان داده شدهاست که حدود ۴۰۰ ژن، ویژه مغز هستند. در همه نورونها ELAVL3[ات] و در نورونهای هرمی NRGN[اث] و REEP2[اج] نیز بیان میشود. GAD1 - ضروری برای بیوسنتز انتقال دهنده عصبی GABA - در بین نورونها بیان میشود. پروتئین بیان شده در سلولهای گلیال شامل نشانگر آستروسیت GFAP[اچ] و S100B[اح] است در حالی که پروتئین اصلی میلین و فاکتور رونویسی OLIG2[اخ] در الیگودندروسیت بیان شدهاست.[۴۶]
مایع مغزی نخاعی ویرایش
مایع مغزی نخاعی یک مایع بین سلولی شفاف و بیرنگ است که در اطراف مغز در شامگان، در دستگاه بطنی و در کانال مرکزی نخاع در گردش است. همچنین برخی از شکافهای فضای زیر عنکبوتیه را پر میکند که به عنوان مخازن زیر عنکبوتیه[اد]شناخته میشوند. [۳۹] چهار بطن، دو بطن جانبی، یک بطن سوم و یک بطن چهارم، همگی حاوی یک شبکه کوروئید هستند که مایع مغزی نخاعی تولید میکند. [۴۱] بطن سوم در خط وسط قرار دارد و به بطنهای جانبی متصل است. [۳۹] یک مجرای منفرد، قنات مغزی بین پونز و مخچه، بطن سوم را به بطن چهارم متصل میکند. [۳۹] سه دهانه مجزا، دریچه میانی و دو روزنه جانبی، مایع مغزی نخاعی را از بطن چهارم به سیسترنا مگنا یکی از مخازن اصلی تخلیه میکند. از اینجا، مایع مغزی نخاعی در اطراف مغز و نخاع در فضای زیر عنکبوتیه، بین ماده عنکبوتیه و پیا ماتر، گردش میکند. [۳۹] در هر زمان، حدود ۱۵۰ میلی لیتر مایع مغزی نخاعی که بیشتر در فضای زیر عنکبوتیه وجود دارد دائماً در حال بازسازی و جذب است و تقریباً هر ۵ تا ۶ ساعت یک بار جایگزین میشود. [۳۹]
سیستم لنفاوی[۴۷][۴۸][۴۹] به عنوان سیستم تخلیه لنفاوی مغز توصیف شدهاست. مسیر گلیمفاتیک در سراسر مغز شامل مسیرهای تخلیه از مایع مغزی نخاعی و از عروق لنفاوی مننژیال[اذ] است که با سینوسهای دورال مرتبط هستند و در کنار رگهای خونی مغز قرار دارند.[۵۰][۵۱] این مسیر مایع بینابینی را از بافت مغز تخلیه میکند.[۵۱]
تأمین خون ویرایش
سرخرگهای کاروتید درونی خون اکسیژن دار را به قسمت جلوی مغز و سرخرگهای مهرهای خون را به پشت مغز میرسانند. [۳۹] این دو گردش خون در حلقه ویلیس به هم می پیوندند، حلقه ای از شریانهای متصل که در مخزن بین ساقه ای بین مغز میانی و پونز قرار دارد. [۳۹]
شریانهای کاروتید داخلی شاخههایی از سرخرگ کاروتید مشترک هستند. آنها از طریق کانال کاروتید [ار] وارد جمجمه میشوند، از طریق سینوس کاورنوس[از] حرکت میکنند و وارد فضای شامگان میشوند. [۳۹] سپس آنها وارد حلقه ویلیس میشوند، با دو شاخه، که از طریق سرخرگ مغزی پیشین بیرون میآیند. این شاخهها در امتداد شکاف طولی به سمت جلو و سپس به سمت بالا حرکت میکنند و قسمت جلویی و خط میانی مغز را تأمین میکنند. [۳۹] یک یا چند سرخرگ ارتباطی پیشین، مدت کوتاهی پس از بیرون آمدن آنها به صورت شاخه به دو شریان مغزی قدامی میپیوندند. [۳۹] شریانهای کاروتید داخلی به عنوان سرخرگ مغزی میانی به جلو پیش میروند. آنها به طرفی در امتداد استخوان پروانهای کاسه چشم حرکت میکنند، سپس از طریق قشر اینسولار، جایی که شاخههای نهایی ایجاد میشوند، به سمت بالا حرکت میکنند. [۳۹]
شریانهای مهره ای به صورت شاخههایی از سرخرگ زیرترقوهای چپ و راست ظاهر میشوند. آنها از طریق سوراخهای عرضی که فضاهایی در مهرههای گردن هستند به سمت بالا حرکت میکنند. هر طرف از طریق فورامن مگنوم در امتداد سمت مربوطه مدولا وارد حفره جمجمه میشود. [۳۹] آنها یکی از سه شاخه مخچه را بیرون میدهند. شریانهای مهرهای در جلوی قسمت میانی مدولا به هم میپیوندند و سرخرگ قاعدهای بزرگتری را تشکیل میدهند که شاخههای متعددی را برای تأمین مدولا و پونز و دو شاخه مخچه قدامی و فوقانی میفرستد. [۳۹] در نهایت، سرخرگ قاعدهای (بازیلار) به دو سرخرگ مغزی پسین تقسیم میشود. اینها به سمت خارج، اطراف دمگلهای مخچه فوقانی و در امتداد بالای تنتوریوم مخچه حرکت میکنند، جایی که شاخههایی را برای تأمین لوبهای گیجگاهی و پس سری میفرستند. [۳۹] هر شریان مغزی خلفی یک سرخرگ ارتباطی پسین کوچک را میفرستد تا به شریانهای کاروتید داخلی بپیوندد.
تخلیه خون ویرایش
سیاهرگهای مغزی[اژ] خون کم اکسیژن را از مغز تخلیه میکنند. مغز دارای دو شبکه اصلی سیاهرگ شامل یک شبکه بیرونی یا سطحی، در سطح مغز که دارای سه شاخه است و یک شبکه داخلی میشود. این دو شبکه از طریق وریدهای آناستوموز (بازپیوندی) با هم ارتباط برقرار میکنند. [۳۹] سیاهرگهای مغز به حفرههای بزرگتر سینوسهای سیاهرگی سختشامه که معمولاً بین سختشیره و پوشش جمجمه قرار دارند، تخلیه میشوند. [۵۲] خون از مخچه و مغز میانی به سیاهرگ بزرگ مغز[اس] تخلیه میشود. خون از بصل النخاع و پونز ساقه مغز دارای الگوی متغیری به وریدهای نخاعی یا وریدهای مغزی مجاور است. [۳۹]
خون در قسمت عمیق مغز از طریق یک شبکه وریدی به سینوس کاورنو در جلو و سینوسهای پتروزال فوقانی و تحتانی در طرفین و سینوس ساژیتال تحتانی در پشت تخلیه میشود. [۵۲] خون از مغز بیرونی به سینوس ساژیتال فوقانی[اش] بزرگ تخلیه میشود که در خط وسط بالای مغز قرار دارد. خون از اینجا به خون سینوس مستقیم[اص] در محل تلاقی سینوسها میپیوندد. [۵۲]
خون از اینجا به سینوسهای عرضی چپ و راست تخلیه میشود. [۵۲] سپس این سینوسها به سینوسهای سیگموئید تخلیه میشوند که خون را از سینوس کاورنووس و سینوسهای خارهای فوقانی و تحتانی دریافت میکنند. سیگموئید به سیاهرگ ژوگولار داخلی تخلیه میشود. [۵۲] [۳۹]
سد خونی مغزی ویرایش
شریانهای بزرگتر در سراسر مغز خون را به مویرگهای کوچکتر میرسانند. این کوچکترین رگهای خونی در مغز، با سلولهایی پوشانده شدهاند که با اتصالات محکم به هم متصل شدهاند و بنابراین مایعات به همان درجهای که در مویرگهای دیگر وجود دارد، داخل یا خارج نمیشوند که باعث ایجاد سد خونی مغزی میشود. [۴۰] پریسیتز[اض] نقش عمده ای در تشکیل اتصالات محکم دارند.[۵۳] این مانع برای مولکولهای بزرگتر نفوذپذیری کمتری دارد، اما همچنان در برابر آب، دیاکسید کربن، اکسیژن و بیشتر مواد محلول در چربی (از جمله بیهوش کنندهها و الکل) نفوذپذیر است. [۴۰] سد خونی مغزی در اندامهای دور بطنی[اط]— که ساختارهایی در مغز هستند که ممکن است نیاز به واکنش به تغییرات در مایعات بدن داشته باشند — مانند غده کاجی، ناحیه پوسترما، و برخی از نواحی هیپوتالاموس وجود ندارد. [۴۰] سد خونی مایع مغزی نخاعی مشابهی وجود دارد که همان هدف سد خونی مغزی را دارد، اما به دلیل ویژگیهای ساختاری متمایز بین دو سیستم مانع، انتقال مواد مختلف به مغز را تسهیل میکند. [۴۰]
رشد ویرایش
در آغاز هفته سوم رشد، اکتودرم جنینی یک نوار ضخیم به نام صفحه عصبی را تشکیل میدهد.[۵۴] در هفته چهارم رشد، صفحه عصبی گشاد شده و یک انتهای سفالیک پهن، یک قسمت میانی کمتر پهن و یک انتهای دمی باریک ایجاد میکند. این تورمها بهعنوان وزیکولهای اولیه مغز شناخته میشوند و نشاندهنده آغاز پیشمغز (پروانسفالون)، میانمغز (مزانسفالون)، و پسمغز (رومبنسفالون) هستند.[۵۵]
سلولهای تاج عصبی (که از اکتودرم مشتق شدهاند) لبههای جانبی صفحه را در چینهای عصبی پر میکنند. در هفته چهارم - در مرحله نورولاسیون - چینهای عصبی نزدیک میشوند تا لوله عصبی را تشکیل دهند و سلولهای تاج عصبی را در محل تاج عصبی به هم نزدیک میکنند.[۵۶] تاج عصبی در طول لوله با سلولهای تاج عصبی جمجمه در انتهای سفالیک و سلولهای تاج عصبی دمی در دم قرار دارد. سلولها از تاج جدا میشوند و در یک موج کرانیوکودال (سر تا دم) در داخل لوله مهاجرت میکنند.[۵۶] سلولهای انتهای سفالیک باعث ایجاد مغز میشوند و سلولهای انتهای دمی باعث ایجاد طناب نخاعی میشوند.[۵۷]
لوله هنگام رشد خم میشود و نیمکرههای مغزی هلالی شکل را در سر تشکیل میدهد. نیمکرههای مغز برای اولین بار در روز ۳۲ ظاهر میشوند.[۵۸] در اوایل هفته چهارم، قسمت سفالیک در خم شدن سفالیک به شدت به جلو خم میشود.[۵۶] این قسمت خم شده به قسمت جلویی مغز تبدیل میشود. قسمت منحنی مجاور به میانمغز (مزانسفالون) و قسمت دمی به خم شدن به پسمغز (رومبنسفالون) تبدیل میشود. این نواحی به صورت تورمهایی به نام سه وزیکول اولیه مغزی تشکیل میشوند. در هفته پنجم رشد، پنج وزیکول مغزی ثانویه تشکیل شدهاست.[۵۹] مغز جلویی به دو وزیکول تقسیم میشود - یک تلانسفالون قدامی و یک دی انسفالون خلفی. تلنسفالون قشر مغز، عقدههای قاعده ای و ساختارهای مرتبط را ایجاد میکند. دی انسفالون باعث ایجاد تالاموس و هیپوتالاموس میشود. مغز عقبی نیز به دو ناحیه متانسفالون و میلنسفالون تقسیم میشود. متانسفالون باعث ایجاد مخچه و پل مغزی میشود. میلنسفالون باعث ایجاد بصل النخاع میشود.[۶۰] همچنین در طول هفته پنجم، مغز به بخشهای تکراری به نام نورومرها تقسیم میشود.[۵۵][۶۱] در مغز عقب اینها به عنوان لوزی شناخته میشوند.[۶۲]
یکی از ویژگیهای مغز چین خوردگی قشری است که به نام چرخش شناخته میشود. برای کمی بیش از پنج ماه از رشد قبل از تولد، قشر صاف است. در سن ۲۴ هفته حاملگی، مورفولوژی چروکیده که شکافهایی را نشان میدهد که شروع به مشخص کردن لوبهای مغز میکند، مشهود است.[۶۳] چرایی چین و چروک و چینخوردگی قشر مغز به خوبی درک نشدهاست، اما ژیفیکاسیون با هوش و اختلالات عصبی مرتبط و تعدادی از تئوریهای ژیریفیکاسیون ارائه شدهاست.[۶۴] این تئوریها شامل آنهایی است که بر اساس کمانش مکانیکی،[۶۵][۶۶] کشش آکسونی،[۶۷] و انبساط مماسی دیفرانسیل است.[۶۸] آنچه واضح است این است که چرخش یک فرایند تصادفی نیست، بلکه یک فرایند پیچیده از پیش تعیین شدهاست که الگوهای چینخوردگی را ایجاد میکند که بین افراد و بیشتر گونهها سازگار است.[۶۹][۷۰]
اولین شیاری که در ماه چهارم ظاهر میشود، حفره جانبی مغز است.[۵۸] انتهای دمی در حال گسترش نیمکره باید در جهت رو به جلو خمیده شود تا در فضای محدود قرار گیرد. این حفره را میپوشاند و آن را به برآمدگی عمیقتری تبدیل میکند که به نام شیار جانبی شناخته میشود و لوب گیجگاهی را مشخص میکند.[۵۸] در ماه ششم شکافهای دیگری تشکیل شدهاند که لوبهای پیشانی، جداری و پس سری را مشخص میکنند.[۵۸] یک ژن موجود در ژنوم انسان (ARHGAP11B) ممکن است نقش مهمی در چرخش و انسفالیزاسیون داشته باشد.[۷۱]
وظایف و عملکرد ویرایش
مغز انسان از ۸۶ میلیارد سلول عصبی تشکیل شدهاست؛ این سیستم به وسیله ارتباط میان بخشهای مختلف بدن مانند دستگاه گردش خون، دستگاه گوارش، سیستم ایمنی و … باعث ایجاد هماهنگی در فعالیتهای بدن میشود.[۷۲] مدارهای حرکتی دستورات را به ماهیچهها برده و رفلکسهای سادهٔ ارادی را ایجاد میکند؛ مدارات حسی پیامها را از گیرندههای حسی دریافت و به سمت مغز هدایت میکند تا پاسخ مناسبی به این پدیدهها داده شود. همچنین فعالیتهای شناختی مانند حافظه، تصمیمگیری و ادراک توسط کورتکس پردازش و فعالیتهای پیچیده مانند زبان و برنامهریزی را ایجاد میکند.[۷۳][۷۴]
کنترل حرکات بدن ویرایش
لوب پیشانی در استدلال، حرکت ارادی، احساس و زبان نقش دارد. این لوب قشر حرکتی[اظ]، قشر پیش پیشانی و منطقه بروکا را نیز شامل میشود. قشر حرکتی مسئول ایجاد، تعادل و هماهنگی حرکات در بدن است؛ قشر پیش پیشانی، مسئول عملکردهای شناختی سطح بالا و پیچیدهاست و منطقه بروکا برای فرایندهای مرتبط با زبان ضروریست[۷۵] و آسیب به آن میتواند بیماریهایی مانند آفازی بروکا را ایجاد کند.[۷۶] مغز به وسیله ارتباط با مخچه پیامهای ارادی و نیمه ارادی را از طریق اعصاب مغزی به نورونهای حرکتی بدن منتقل و به وسیله مجرای نخاعی پیامهای حرکتی را از مغز، به دیگر بخشهای بدن و اندامها ارسال میکند.[۷۷] اعصاب اطراف جمجمه نیز حرکات مربوط به چشم، دهان و صورت را بدون واسطه تنظیم و هماهنگ میکند.[۷۸]
حرکتهای درشت، مانند حرکت بدن، حرکت بازوها و پاها، در قشر حرکتی ایجاد میشود. این بخش دارای سه قسمت است:[۷۹][۸۰]
- قشر حرکتی اولیه که بخشی از شکنج پیش مرکزی[اع] بوده و دارای بخشهایی است که به حرکت قسمتهای مختلف بدن اختصاص دارد.
- ناحیه پیش حرکتی[اغ] که در جلوی قشر حرکتی اولیه قرار دارد و در تنظیم و هماهنگ سازی حرکات نقش اساسی ایفا میکند.
- ناحیه حرکتی تکمیلی[اف] که در مجاور ناحیه پیش حرکتی قرار دارد و همانند آن وظیفه هماهنگ سازی و تنظیم حرکات بدن را بر عهده دارد.
دستها و دهان نسبت به سایر قسمتهای بدن ناحیه بسیار بزرگتری از مغز را برای پردازش اطلاعات حرکتی شان در اختیار دارند همین امر سبب میشود قادر به انجام حرکتهای ظریف و پیچیده تری مانند تکلم و نوشتن شوند.[۸۱] پیامهای عصبی تولید شده از قشر حرکتی در امتداد دستگاه کورتیکوسپینال[اق] در جلوی بصل النخاع حرکت کرده و با گذر از اهرام مدولاری[اک] و مقطع عرضی بصل النخاع در سطح تقاطع هرمها، وارد ریشه پشتی در کانال نخاعی میشود و از طریق نورونهای حرکتی پیامهای انقباضی را برای ماهیچهها ارسال میکند. مخچه و عقدههای قاعده ای نیز در تنظیم حرکات ظریف و پیچیده عضلات نقش دارند.[۸۲][۸۳]
به وسیلهٔ همونکلوس حرکتی[اگ] بخشهای درگیرِ مغز در حرکت هر کدام از اندامهای بدن را توصیف میکنند.[۷۹]
درک حواس بدن ویرایش
سیستم عصبی حسی وظیفه دریافت و پردازش اطلاعات حسی را بر عهده دارد. این اطلاعات از طریق اعصاب جمجمه، از طریق مجاری در طناب نخاعی و مستقیماً در مراکزی از مغز دریافت میشود که به وسیلهٔ رگهای مجاور عصب خون رسانی میشوند.[۸۴] موتورهای ترکیبی و سیگنالهای حسی نیز یکپارچه شدهاند.[۸۴]
مغز اطلاعات مربوط به لمس ظریف، فشار، درد، لرزش و دما را از پوست دریافت میکند. از مفاصل، مغز اطلاعاتی در مورد موقعیت مفصل دریافت میکند.[۸۵] قشر حسی دقیقاً در نزدیکی قشر حرکتی قرار دارد و مانند قشر حرکتی دارای نواحی مربوط به احساس از قسمتهای مختلف بدن است. حسی که توسط یک گیرنده حسی روی پوست جمعآوری میشود به یک سیگنال عصبی تبدیل میشود که از طریق دستگاههای نخاعی به تعدادی نورون منتقل میشود. مسیر ستون پشتی-لمنیسکوس داخلی حاوی اطلاعاتی در مورد لمس ظریف، ارتعاش و موقعیت مفاصل است. فیبرهای مسیر از قسمت پشتی نخاع به قسمت پشتی بصل النخاع میروند، جایی که با نورونهای مرتبه دوم متصل میشوند که بلافاصله الیاف را در سراسر خط وسط میفرستند. این فیبرها سپس به سمت بالا به داخل کمپلکس شکمی بازال[ال] در تالاموس حرکت میکنند، جایی که با نورونهای مرتبه سوم که فیبرها را به قشر حسی میفرستند، متصل میشوند.[۸۵] دستگاه اسپینوتلامیک[ام] اطلاعاتی در مورد درد، دما و لمس شدید دارد. فیبرهای مسیر از طناب نخاعی عبور میکنند و با نورونهای مرتبه دوم در تشکیل شبکهای ساقه مغز برای درد و دما متصل میشوند و همچنین برای لمس شدید به کمپلکس شکمی تالاموس ختم میشوند.[۸۶]
بینایی توسط نوری که به شبکیه چشم برخورد میکند تولید میشود. گیرندههای نوری در شبکیه، محرک حسی نور را به سیگنال عصبی الکتریکی منتقل میکنند که به قشر بینایی در لوب پس سری فرستاده میشود. سیگنالهای بینایی از طریق اعصاب بینایی شبکیه را ترک میکنند. فیبرهای عصبی بینایی از نیمههای بینی شبکیه به طرف مقابل میپیوندند و از نیمههای زمانی شبکیه مقابل به فیبرها میپیوندند تا مجاری بینایی را تشکیل دهند. ترتیب اپتیک چشم و مسیرهای بینایی به این معنی است که دید از میدان بینایی چپ توسط نیمه راست هر شبکیه دریافت میشود، توسط قشر بینایی سمت راست پردازش میشود و بالعکس. فیبرهای مجرای بینایی در هسته ژنیکوله جانبی به مغز میرسند و از طریق تشعشعات بینایی برای رسیدن به قشر بینایی حرکت میکنند.[۸۷]
شنوایی و تعادل هر دو در گوش داخلی ایجاد میشوند. صدا منجر به ارتعاشات استخوانچهها میشود که در نهایت به اندام شنوایی ادامه مییابد و تغییر در تعادل منجر به حرکت مایعات در گوش داخلی میشود. این یک سیگنال عصبی ایجاد میکند که از عصب دهلیزی عبور میکند. از اینجا به هستههای حلزونی، هسته اولیواری فوقانی، هسته ژنیکوله داخلی و در نهایت تابش شنوایی به قشر شنوایی میرسد.[۸۸]
حس بویایی توسط سلولهای گیرنده در اپیتلیوم مخاط بویایی در حفره بینی ایجاد میشود. این اطلاعات از طریق عصب بویایی که از طریق قسمت نسبتاً قابل نفوذ به جمجمه میرود منتقل میشود. این عصب به مدار عصبی لامپ بویایی منتقل میشود و از آنجا اطلاعات به قشر بویایی منتقل میشود.[۸۹][۹۰] مزه از گیرندههای روی زبان ایجاد میشود و در امتداد اعصاب صورت و گلوفارنکس به هسته منفرد در ساقه مغز منتقل میشود. برخی از اطلاعات چشایی نیز از طریق عصب واگ از حلق به این ناحیه منتقل میشود. سپس اطلاعات از اینجا از طریق تالاموس به قشر چشایی منتقل میشود.[۹۱]
تنظیم ویرایش
عملکردهای خودمختار مغز شامل تنظیم یا کنترل ریتمیک ضربان قلب و تعداد تنفس و حفظ هموستازی است.[۹۲]
فشار خون و ضربان قلب تحت تأثیر مرکز وازوموتور بصل النخاع است که باعث میشود سرخرگها و سیاهرگها در حالت استراحت تا حدودی منقبض شوند. این کار را با تأثیرگذاری بر سیستم عصبی سمپاتیک و پاراسمپاتیک از طریق عصب واگ انجام میدهد. اطلاعات مربوط به فشار خون توسط بارورسپتورها در اجسام آئورت در قوس آئورت تولید میشود و در امتداد رشتههای آوران عصب واگ به مغز منتقل میشود.[۹۲] اطلاعات مربوط به تغییرات فشار در سینوس کاروتید از اجسام کاروتید واقع در نزدیکی سرخرگ کاروتید بدست میآید و از طریق یک عصب که به عصب گلوسوفارنکس میپیوندد منتقل میشود. این اطلاعات به سمت هسته منفرد در بصل النخاع میرود. سیگنالها از اینجا بر مرکز وازوموتور تأثیر میگذارند تا انقباض سیاهرگ و سرخرگ را متناسب با آن تنظیم کند.[۹۳]
مغز سرعت تنفس را عمدتاً توسط مراکز تنفسی در مدولا و پونز کنترل میکند.[۹۴] مراکز تنفسی با تولید سیگنالهای حرکتی که از طناب نخاعی، در امتداد عصب فرنیک به دیافراگم و سایر عضلات تنفسی منتقل میشوند، تنفس را کنترل میکنند. این یک عصب مختلط است که اطلاعات حسی را به مراکز برمیگرداند. چهار مرکز تنفسی وجود دارد، سه مرکز با عملکرد واضحتر و یک مرکز آپنوستی با عملکرد کمتر مشخص. در بصل النخاع، یک گروه تنفسی پشتی باعث میل به تنفس میشود و اطلاعات حسی را مستقیماً از بدن دریافت میکند. همچنین در بصل النخاع، گروه تنفسی شکمی بر بازدم در حین فعالیت تأثیر میگذارد. در پونز، مرکز پنوموتاکسیک[ان] بر مدت زمان هر تنفس تأثیر میگذارد،[۹۴] و به نظر میرسد مرکز آپنوستیک بر استنشاق تأثیر میگذارد. مراکز تنفسی بهطور مستقیم کربن دیاکسید و pH خون را حس میکنند. اطلاعات مربوط به اکسیژن خون، دیاکسید کربن و سطوح pH نیز بر روی دیواره سرخرگها در گیرندههای شیمیایی محیطی بدن آئورت و کاروتید حس میشود. این اطلاعات از طریق اعصاب واگ و گلوسوفارنکس به مراکز تنفسی منتقل میشود.[۹۴] دیاکسید کربن بالا، PH اسیدی یا اکسیژن کم، مراکز تنفسی را تحریک میکند. میل به تنفس نیز تحت تأثیر گیرندههای کششی ریوی در ششها قرار میگیرد که وقتی فعال میشوند، با انتقال اطلاعات به مراکز تنفسی از طریق عصب واگ، از باد کردن بیش از حد ششها جلوگیری میکنند.[۹۴]
هیپوتالاموس در دی انسفالون، در تنظیم بسیاری از عملکردهای بدن نقش دارد. عملکردها شامل تنظیم عصبی غدد درون ریز، تنظیم ریتم شبانهروزی، کنترل دستگاه عصبی خودمختار، و تنظیم مایعات و مصرف غذا است. ریتم شبانهروزی توسط دو گروه سلولی اصلی در هیپوتالاموس کنترل میشود. هیپوتالاموس قدامی شامل هسته سوپراکیاسماتیک و هسته پره اپتیک بطنی جانبی است که از طریق چرخههای بیان ژن، یک ساعت شبانهروزی تقریباً ۲۴ ساعته ایجاد میکند. در روز شبانهروزی، یک ریتم اولترادیا کنترل الگوی خواب را به دست میگیرد. خواب یک نیاز ضروری برای بدن و مغز است و باعث بسته شدن و استراحت سیستمهای بدن میشود.[۹۵] همچنین یافتههایی وجود دارد که نشان میدهد تجمع روزانه سموم در مغز در طول خواب حذف میشود. در هنگام بیداری مغز یک پنجم کل انرژی مورد نیاز بدن را مصرف میکند. خواب لزوماً این استفاده را کاهش میدهد و برای بازیابی ATP انرژی زا زمان میدهد. آثار کم خوابی نیاز مطلق به خواب را نشان میدهد.[۹۶]
هیپوتالاموس جانبی حاوی نورونهای اورکسینرژیک است که اشتها و برانگیختگی را از طریق پیشبینی خود به سیستم فعال کننده شبکه صعودی کنترل میکنند.[۹۷][۹۸] هیپوتالاموس غده هیپوفیز را از طریق انتشار پپتیدهایی مانند اکسی توسین و وازوپرسین و همچنین دوپامین در برجستگی میانه کنترل میکند. از طریق برجستگیهای اتونومیک، هیپوتالاموس در تنظیم عملکردهایی مانند فشار خون، ضربان قلب، تنفس، تعریق و سایر مکانیسمهای هموستاتیک نقش دارد.[۹۹] هیپوتالاموس همچنین در تنظیم حرارتی نقش دارد و هنگامی که توسط سیستم ایمنی تحریک شود، قادر به ایجاد تب است. هیپوتالاموس تحت تأثیر کلیهها قرار میگیرد: هنگامی که فشار خون کاهش مییابد، رنین آزاد شده توسط کلیهها نیاز به نوشیدن را تحریک میکند. هیپوتالاموس همچنین مصرف غذا را از طریق سیگنالهای خودمختار و ترشح هورمون توسط دستگاه گوارش تنظیم میکند.[۱۰۰]
زبان ویرایش
در حالی که به گذشته تصور میشد که بخش پردازش کننده زبان در ناحیه ورنیکه و بروکا است،[۱۰۱] اکنون اکثراً پذیرفته شدهاست که شبکه گستردهتری از مناطق قشر مغز به عملکردهای زبان کمک میکند.[۱۰۲][۱۰۳][۱۰۴]
مطالعه در مورد چگونگی بازنمایی، پردازش و کسب زبان توسط مغز، عصب-زبانشناسی نامیده میشود که یک حوزه چندرشتهای بزرگ است که از علوم اعصاب شناختی، زبانشناسی شناختی، و روانزبانشناسی استخراج میشود.[۱۰۵]
تقسیمبندی وظایف ویرایش
مخ دارای یک سازمان متقابل است که هر نیمکره مغز عمدتاً با نیمی از بدن در تعامل است، سمت چپ مغز با سمت راست بدن، اتصالات حرکتی از مغز به نخاع و اتصالات حسی از نخاع به مغز، هر دو طرف متقاطع در ساقه مغز با یکدیگر تعامل دارد و بالعکس. علت تکوینی این امر نامشخص است.[۱۰۶] ورودی بصری از قانون پیچیدهتری پیروی میکند: اعصاب بینایی از دو چشم در نقطهای به نام کیاسما بینایی به هم میرسند و نیمی از رشتههای هر عصب برای پیوستن به دیگری جدا میشوند.[۱۰۷] نتیجه این است که اتصالات نیمه چپ شبکیه، در هر دو چشم، به سمت چپ مغز میرود، در حالی که اتصالات از نیمه راست شبکیه به سمت راست مغز میرود.[۱۰۸] از آنجا که هر نیمه شبکیه نوری را دریافت میکند که از نیمه مخالف میدان بینایی میآید، نتیجه عملکردی این است که ورودی بصری از سمت چپ جهان به سمت راست مغز میرود و بالعکس.[۱۰۶] بنابراین، سمت راست مغز ورودی حسی جسمی را از سمت چپ بدن، و ورودی بینایی را از سمت چپ میدان بینایی دریافت میکند.[۱۰۹][۱۱۰]
سمت چپ و راست مغز متقارن به نظر میرسند، اما به صورت نامتقارن عمل میکنند.[۱۱۱] به عنوان مثال، همتای ناحیه حرکتی نیمکره چپ که دست راست را کنترل میکند، ناحیه نیمکره راست کنترلکننده دست چپ است. با این حال، چندین استثنا مهم وجود دارد که شامل زبان و شناخت فضایی میشود. لوب پیشانی چپ برای زبان غالب است. اگر یک ناحیه کلیدی زبان در نیمکره چپ آسیب ببیند، ممکن است قربانی را قادر به صحبت کردن یا درک نکند،[۱۱۱] در حالی که آسیب معادل به نیمکره راست تنها باعث آسیب جزئی در مهارتهای زبانی میشود.
بخش قابل توجهی از درک کنونی از تعاملات بین دو نیمکره از مطالعه «بیماران دوشاخه مغز» افرادی که در تلاش برای کاهش شدت تشنجهای صرع تحت عمل جراحی برش جسم پینه ای قرار گرفتند، به دست آمدهاست.[۱۱۲] این بیماران رفتار غیرمعمولی را نشان نمیدهند که بلافاصله آشکار شود، اما در برخی موارد میتوانند تقریباً مانند دو فرد مختلف در یک بدن رفتار کنند، با دست راست و سپس دست چپ آن را باز میکند.[۱۱۳][۱۱۴] این بیماران هنگامی که بهطور خلاصه تصویری در سمت راست نقطه تثبیت بینایی نشان داده میشود، قادر به توصیف شفاهی آن هستند، اما زمانی که تصویر در سمت چپ نشان داده میشود، قادر به توصیف آن نیستند، اما ممکن است قادر به ارائه نشانه باشند. با دست چپ ماهیت شی نشان داده شدهاست.[۱۱۵][۱۱۶]
عواطف ویرایش
عواطف عموماً به عنوان فرآیندهای چند جزئی دو مرحله ای شامل برانگیختن و به دنبال آن احساسات روانشناختی، ارزیابی، بیان، پاسخهای خودمختار و تمایلات عملی تعریف میشوند.[۱۱۷] تلاش برای بومی سازی احساسات اساسی در مناطق خاصی از مغز بحثبرانگیز بودهاست. برخی از تحقیقات هیچ مدرکی برای مکانهای خاص مربوط به احساسات پیدا نکردند، اما در عوض مدارهایی را درگیر در فرآیندهای عاطفی عمومی یافتند. به نظر میرسد آمیگدال، قشر چشمخانهایپیشانی (اوربیتوفرونتال)، قشر اینسولا میانی و قدامی و قشر پیش پیشانی جانبی در ایجاد احساسات دخیل هستند، در حالی که شواهد ضعیف تری برای ناحیه تگمنتال شکمی، رنگپریدگی شکمی و هسته اکومبنس در برجستگی انگیزشی یافت شد.[۱۱۸] با این حال، برخی دیگر شواهدی مبنی بر فعال شدن نواحی خاص، مانند عقدههای قاعده ای در شادی، قشر سینگولیت ساب پینه ای در غم و آمیگدال در ترس یافتهاند.[۱۱۹]
شناخت ویرایش
مغز مسئول شناخت است،[۱۲۰][۱۲۱] که از طریق فرآیندهای متعدد و عملکردهای اجرایی عمل میکند.[۱۲۲][۱۲۳][۱۲۴] عملکردهای اجرایی شامل توانایی فیلتر کردن اطلاعات و تنظیم محرکهای نامربوط با کنترل توجه و بازداری شناختی، توانایی پردازش و دستکاری اطلاعات ذخیره شده در حافظه کاری، توانایی فکر کردن به چندین مفهوم بهطور همزمان و تغییر وظایف با انعطافپذیری شناختی، توانایی با کنترل بازدارنده، و توانایی تعیین ارتباط اطلاعات یا تناسب یک عمل، از تکانهها و پاسخهای قوی جلوگیری میکند.[۱۲۳][۱۲۴] کارکردهای اجرایی مرتبه بالاتر مستلزم استفاده همزمان از چندین کارکرد اجرایی اساسی است و شامل برنامهریزی، آینده نگری و هوش سیال (یعنی استدلال و حل مسئله) میشود.[۱۲۴]
قشر جلوی مغز نقش مهمی در میانجیگری عملکردهای اجرایی دارد.[۱۲۲][۱۲۴][۱۲۵] برنامهریزی شامل فعالسازی قشر پیش پیشانی پشتی جانبی (DLPFC)، قشر کمربندی قدامی، قشر جلوی پیشانی زاویهدار، قشر جلوی پیشانی راست و شکنج فوقمارژینال است.[۱۲۵] دستکاری حافظه کاری شامل DLPFC، شکنج فرونتال تحتانی و نواحی قشر جداری میشود.[۱۲۲][۱۲۵] کنترل مهاری شامل چندین نواحی از قشر جلوی مغز و همچنین هسته دمی و هسته زیر تالاموس میشود.[۱۲۴][۱۲۵][۱۲۶]
پژوهش ویرایش
مغز بهطور کامل درک نشدهاست و تحقیقات بر روی آن همچنان در حال انجام است.[۱۲۷] امروزه دانشمندان علوم اعصاب و محققانی از رشتههای دیگر، چگونگی کارکرد مغز انسان را مطالعه میکنند. مرزهای بین تخصصهای علوم اعصاب، عصبشناسی و سایر رشتهها مانند روانپزشکی، دیگر وجود ندارد زیرا همه آنها بخشی از پژوهشهای بنیادی مرتبط با علوم اعصاب بهشمار میآیند که به بررسی فرایندهای موجود در مغز میپردازد.[۱۲۸][۱۲۹]
پژوهشهای علوم اعصاب در دهههای اخیر بهطور قابل توجهی گسترش یافتهاست. «دهه مغز»[او]، طرح پیشنهاد شده توسط ایالات متحده در دهه ۱۹۹۰ بود که موجب افزایش تحقیقات در این زمینه شد[۱۳۰] و در سال ۲۰۱۳ توسط «طرح ابتکار مغز» دنبال شد.[۱۳۱] پروژه ارتباط انسانی، از دیگر طرحهای تحقیقاتی مرتبط با مغز، از سال ۲۰۰۹ به مدت پنج سال ادامه داشت و اطلاعات مفیدی در رابطه با اتصالات آناتومیکی و کارکردی بخشهای مغز ارائه کرد.[۱۲۷]
روشها ویرایش
دادههای مربوط به ساختار و کارکرد مغز انسان از روشهای آزمایشی گوناگون، روی جانوران و انسانها به دست میآید. اطلاعات بیماران مبتلا به ضربه و سکته مغزی اطلاعاتی در مورد عملکرد بخشهایی از مغز و اثرات آسیب مغزی ارائه کردهاست. تصویربرداری عصبی برای تجسم مغز و ثبت فعالیت مغز و الکتروفیزیولوژی برای اندازهگیری، ثبت و نظارت بر فعالیت الکتریکی قشر مغز مورد استفاده قرار میگیرد. اندازهگیریها ممکن است بر روی پتانسیل میدانی موضعی قشر مغز یا بر روی تنها یک نورون صورت پذیرد. از گرفتن نوار مغزی نیز برای ثبت فعالیت الکتریکی قشر مغز استفاده میشود؛ در این روش با استفاده از الکترودهایی که به صورت غیر مخرب روی پوست سر قرار دارد، سیگنالهای ارسالی، ناشی از کارکرد مغز، ثبت و آنالیز میشود.[۱۳۲] [۴۱]
روشهای مخرب و آسیب زا نیز برای پژوهش بر روی مغز وجود دارد، یکی از این موارد الکتروکورتیکوگرافی (ECoG) است. در ECoG از الکترودهایی استفاده میشود که مستقیماً روی سطح مغز قرار میگیرند. از این روش برای نقشهبرداری تحریکی قشر مغز[اه]، مطالعه رابطه بین نواحی قشر مغز و کارکرد سیستمیک آنها استفاده میشود.[۱۳۳] همچنین میتوان با استفاده از میکروالکترودهای کوچکتری ضبطهای تک واحدی[ای] را از یک نورون منفرد انجام داد که وضوح فضایی و زمانی بالایی را از فعالیت مغز ارائه میدهند. این روشِ اسکن مغزی امکان بررسی ارتباطِ بین فعالیت مغز با رفتار و ایجاد نقشههای عصبی را فراهم کردهاست.[۱۳۴] گسترش ارگانوئیدهای مغزی راههایی را برای مطالعه بیشتر، بر روی فرایندهای مرتبط با مغز مانند رشد، تکامل، پلاستیسیته و بیماریهایی نظیر دمانس، اماس، صرع و … ایجاد نمودهاست.[۱۳۵][۱۳۶]
تصویربرداری ویرایش
تکنیکهای تصویربرداری عصبی کارکردی تغییراتی را در فعالیت مغز نشان میدهند که به عملکرد نواحی خاص مغز مربوط میشود. یکی از روشهای افامآرآی است که نسبت به روشهای پیشین چون مقطعنگاری رایانهای تکفوتونی و برشنگاری با گسیل پوزیترون مزیتهای بیشتری دارد که به استفاده از مواد رادیواکتیو نیاز ندارد و وضوح بالاتری از فعالیتها و ساختارهای مغز ارائه میدهد.[۱۳۷] روش دیگر طیفنگاری کارکردی فروسرخ نزدیک است. این روشها بر پاسخ همودینامیک[با] متکی هستند و اطلاعاتی از مغز که با تغییرات جریان خون مرتبط اند نشان میدهند.[۱۳۸] تصویر برداری مغز در نگاشت از عملکردهای مناطق مختلف مغز بسیار مفید است و اطلاعات مهمی را در اختیار محققان قرار میدهد.[۱۳۹] دیگر روش تصویر برداری، افامآرآی حالت استراحت، به بررسی تعامل بخشهای مختلف مغز در زمان استراحت (زمانی که فعالیت خاصی انجام نمیدهد مانند خواب) میپردازد. این روش همچنین برای نشان دادن شبکه حالت پیشفرض نیز مورد استفاده قرار میگیرد.[۱۴۰]
هر جریان الکتریکی یک میدان مغناطیسی ایجاد میکند. نوسانات عصبی داخل مغز نیز، میدانهای مغناطیسی ضعیفی را تشکیل میدهند که مگنتوانسفالوگرافی میتواند با استفاده از آن، تصویری از فعالیت موضعی مغز با وضوح بالا نشان دهد.[۴۱] تراکتوگرافی از امآرآی و آنالیز تصویر برای ایجاد تصاویر سه بعدی از تنه عصبی مغز استفاده میکند.[۱۴۱] کانکتوگرام دستگاه دیگری است که یک نمایش گرافیکی از اتصالات عصبی مغز را ارائه میدهند.[۱۳۹]
تفاوت در ساختار مغز[بب] را میتوان در برخی از اختلالات، به ویژه اسکیزوفرنی و زوال عقل، نسبت به حالت طبیعی به وسیلهٔ روشهای تصویربرداری اندازهگیری کرد. یکی از منابع کلیدی جمعآوری اطلاعات در مورد عملکرد نواحی مغز، بررسی موارد آسیب دیده آن بخشها است. همچنین رویکردهای زیستشناختی مختلف با استفاده از تصویربرداری، درک بهتری را در مواردی مانند اختلالات افسردگی و اختلال وسواس فکری-جبری به محققان دادهاست. پیشرفتها در تصویربرداری عصبی، بینش عینی را در مورد اختلالات روانی امکانپذیر کردهاست که منجر به تشخیص سریعتر، پیشآگهی دقیقتر و نظارت بهتر میشود.[۱۴۲]
بیان ژن و پروتئین ویرایش
بیوانفورماتیک رشتهای از مرتبط با زیستشناسی مولکولی است که شامل تکنیکهای محاسباتی و آماری است و میتواند در مطالعات مغز انسان بهویژه در زمینههای بیان ژن و پروتئین مورد استفاده قرار گیرد.[۱۴۳] این رشته توانسته توالی ژنوم بسیاری از موجودات را شناسایی کند و درک بیشتر از ساختار مغز به محققان بدهد.[۱۴۴] بیوانفورماتیک، مطالعات ژنومیک، ژنومیک عملکردی، حاشیهنویسی دیانای، فناوریهای رونویسی و شناسایی ژنها امکان پژوهش بیشتر بر روی مغز را فراهم آورد و باعث شد مکان و عملکرد بسیاری از ژنها مغز مورد بررسی قرار گیرد.[۱۴۵][۱۴۶][۱۴۷]
تا سال ۲۰۱۷، کمتر از ۲۰۰۰۰ ژن کد کننده پروتئین در انسان بیان شد بود،[۱۴۵] و حدود ۴۰۰ مورد از این ژنها، مختص مغز تشخیص داده شدند.[۱۴۸][۱۴۹] دادههایی که در مورد بیان ژن در مغز ارائه شدهاست به تحقیقات بیشتر در مورد تعدادی از اختلالات کمک کردهاست. به عنوان مثال، استفاده طولانی مدت از الکل، بیان ژنِ تغییر یافته و تغییرات خاص سلولی در مغز را نشان دادهاست که ممکن است به اختلال مصرف الکل وابستگی داشته باشد.[۱۵۰] این تغییرات در ترنسکریپتومیکس سیناپسی در قشر جلوی مغز مشاهده شدهاست و به عنوان عاملی برای وابستگی به الکل و همچنین سایر سوءمصرفهای مواد دیده میشود.[۱۵۱]
سایر مطالعات وابسته نیز شواهدی از تغییرات سیناپسی و از بین رفتن آنها در پیری مغز را آشکار نمودهاست. تغییرات در بیان ژن، سطوح پروتئینها را در مسیرهای عصبی مختلف تغییر میدهد که در اختلال عملکرد یا از دست دادن تماس سیناپسی بسیار مشهود است. این اختلال بر بسیاری از ساختارهای مغز تأثیر میگذارد و تأثیر قابل توجهی بر نورونهای بازدارنده دارد که منجر به کاهش سطح انتقال عصبی و به دنبال آن زوال شناختی و بیماری میشود.[۱۵۲][۱۵۳]
فیزیولوژی ویرایش
انتقال عصبی ویرایش
فعالیت مغز در اثر تعامل و فعالیتهای پیچیده نورونها شکل گرفتهاست. این تعامل و هماهنگی موجب شده انسان غالب بر ۱۰۶ بیت اطلاعات را در هر ثانیه به صورت خود آگاه پردازش کند.[۱۵۴] در صورت ایجاد اختلال در فعالیت نورونها، ممکن است اختلالاتی همچون صرع و آلودینیا ایجاد شود.[۱۵۵] نورون از جسم سلولی، آکسون و دندریت تشکیل شدهاست. دندریتها اغلب شاخههای گستردهای هستند که اطلاعات را به صورت پیام عصبی از پایانههای آکسون[بپ] سایر نورونها یا به صورت گیرنده پیامهای محرکهای محیطی را دریافت میکنند. (گیرندههای درد و فشار)[۱۵۶][۴۲] سیگنالهای دریافتی ممکن است باعث شود، نورون یک پتانسیل عمل (سیگنال الکتروشیمیایی یا تکانه عصبی) را از طریق آکسون خود به پایانه آکسونی ارسال و از طریق فضایی به نام سیناپس آن را به دندریتها یا جسم سلولی نورون بعد از خود منتقل کند.[۱۵۷][۱۵۸] یک پتانسیل عمل غالباً در بخش اولیه آکسون، که شامل مجموعه ای تخصصی از پروتئینها است، آغاز میشود. هنگامی که یک پتانسیل عمل به پایانه آکسونی میرسد، باعث آزاد شدن انتقال دهندههای عصبی واقع در وزیکولهایی (ترشح به صورت اگزوسیتوز) در سیناپس شده و با اتصال به گیرندههایشان در نورونهای پس سیناپسی، اختلاف پتانسیل را در این نورونها تغییر میدهند.[۱۵۹] این انتقال دهندههای عصبی شیمیایی (ناقلین عصبی) دوپامین، سروتونین، GABA، گلوتامات و استیل کولین را شامل میشوند.[۴۲][۱۶۰] GABA اصلیترین انتقال دهنده عصبی بازدارنده و گلوتامات اصلیترین انتقال دهنده عصبی تحریکی در مغز است.[۱۶۱] نورونها در سیناپسها با هم ارتباط بر قرار میکنند و مسیرهای عصبی، مدارهای عصبی و سیستمهای پیچیده بزرگ مانند شبکه برجسته[بت] و شبکه حالت پیش فرض[بث] را تشکیل میدهند که فعالیت بین آنها توسط فرآیند انتقال عصبی هدایت میشود.[۱۶۲]
متابولیسم ویرایش
مغز بیش از ۲۰ درصد از انرژی مورد استفاده بدن انسان را، بیش از هر اندامی دیگر، مصرف میکند.[۱۶۳] در انسان، گلوکز موجود در خون منبع اصلی تأمین انرژی بیشتر سلولهای بدن است و برای انجام عملکردهای طبیعی در بسیاری از بافتها، از جمله مغز، حیاتی است.[۱۶۴] متابولیسم مغز بهطور معمول به گلوکز خون به عنوان یک منبع انرژی متکی است، اما در زمان پایین بودن گلوکز خون (مانند ابتدای صبح، حین ورزشهای استقامتی یا مصرف محدود کربوهیدرات)، مغز از اجسام کتونی و مقدار کمتری گلوکز به عنوان سوخت استفاده میکند؛ همچنین میتواند از لاکتات در حین ورزش برای تأمین انرژی خود استفاده کند.[۱۶۵] مغز گلوکز را به شکل گلیکوژن، در مقادیر بسیار کمتر نسبت به کبد و ماهیچههای اسکلتی، ذخیره میکند.[۱۶۶] اسیدهای چرب بلند زنجیر نمیتوانند از سد خونی-مغزی عبور کنند، به همین دلیل کبد آنها را تجزیه کرده و اجسام کتونی تولید کند؛[۱۶۷] با این حال، اسیدهای چرب کوتاه زنجیر (به عنوان مثال اسید بوتیریک، پروپیونیک اسید و استیک اسید) و اسیدهای چرب با زنجیرهٔ متوسط (مانند اکتانوئیک اسید و هپتانوئیک اسید)، میتوانند از سد خونی مغزی عبور کرده و توسط سلولهای مغزی متابولیزه شوند.[۱۶۸][۱۶۹]
اگرچه مغز انسان تنها ۲٪ از وزن بدن را شامل میشود، اما ۱۵٪ از حجم خون خروجی قلب، ۲۰٪ از کل اکسیژن مصرفی بدن و ۲۵٪ از کل گلوکز بدن را دریافت میکند.[۱۷۰] مغز بیشتر از گلوکز برای انرژی استفاده میکند و محرومیت از گلوکز، همان گونه که در هیپوگلیسمی اتفاق میافتد، میتواند منجر به از دست دادن هوشیاری شود.[۱۷۱] مصرف انرژیِ مغز در طول زمان تغییر زیادی نمیکند، اما مناطق فعال مغز، مانند کورتکس، انرژی بیشتری نسبت دیگر مناطق مغز مصرف میکنند؛ که اساس روشهای تصویربرداریِ عصبیِ عملکردیِ برشنگاری با گسیل پوزیترون و افامآرآی است.[۱۷۲] این روشهای تصویربرداری، تصویری سه بعدی از فعالیت متابولیک مغز ارائه میدهند.[۱۷۳] مطالعات اولیه نشان داد که فعالیتهای متابولیکی مغزِ انسان در حدود پنج سالگی به حداکثر خود میرسد.[۱۷۴]
عملکرد خواب بهطور کامل درک نشدهاست؛ با این حال، شواهدی وجود دارد که نشان میدهد خواب در پاکسازی مواد زائد متابولیکی، استراحت و ترمیم مغز، تثبیت حافظه و تنظیم ناقلهای عصبی مؤثر است و بی خوابی بیش از حد میتواند، همانند نوشیدن الکل، فرایندهای عصبی را مختل کند.[۴۹][۱۷۵][۱۷۶] شواهد نشان میدهد که افزایش پاکسازی مواد زائد متابولیکی در طول خواب از طریق افزایش عملکرد سیستم گلیمپاتیک[بج] رخ میدهد.[۴۹]خواب همچنین ممکن است با تضعیف ارتباطات غیر ضروری (هرس سیناپسی) بر تنظیم و تثبیت عملکردهای شناختی تأثیر بگذارد.[۱۷۷]
اهمیت بالینی ویرایش
آسیب مغز ویرایش
آسیب به مغز میتواند به شکلهای گوناگونی نمایان گردد. ضربه مغزی، به عنوان مثال در ورزشهای برخوردی، پس از سقوط، یا تصادف رانندگی یا کار، میتواند با مشکلات فوری و بلند مدت همراه باشد. مشکلات فوری ممکن است شامل خونریزی در مغز باشد، این اسیبدیدگی ممکن است بافت مغز را فشرده کرده یا به خونرسانی آن آسیب برساند. ممکن است کبودی در مغز ایجاد شود. کبودی ممکن است باعث آسیب گسترده به مجاری عصبی شود که میتواند منجر به وضعیت آسیب آکسون[بچ] شود.[۱۷۸] شکستگی جمجمه[بح]، آسیب به ناحیه ای خاص، ناشنوایی و ضربه مغزی نیز از جمله آسیبهای احتمالی هستند. علاوه بر محل آسیب، طرف مقابل مغز نیز ممکن است تحت تأثیر قرار گیرد که به آن آسیب پیشانی[بخ] میگویند. مسائل طولانی مدت که ممکن است ایجاد شوند شامل اختلال اضطراب پس از سانحه و آب آوردن مغز است. انسفالوپاتی تروماتیک مزمن میتواند به دنبال آسیبهای ترومای سر ایجاد شود.[۱۷۹]
زوال عصبی ویرایش
بیماریهای تخریبکننده عصبی منجر به آسیب پیشرونده به قسمتهای مختلف عملکرد مغز میشود و با افزایش سن بدتر میشود. نمونههای رایج شامل زوال عقل مانند بیماری آلزایمر، زوال عقل الکلی یا زوال عقل عروقی است. بیماری پارکینسون؛ و سایر علل نادر عفونی ، ژنتیکی یا متابولیک مانند بیماری هانتینگتون، بیماریهای نورون حرکتی، اختلالات شناختی مرتبط با ایدز، زوال عقل ناشی از سفلیس و بیماری ویلسون از دیگر بیماریهای این دسته بهشمار میروند. بیماریهای تخریبکننده عصبی میتوانند قسمتهای مختلف مغز را تحت تأثیر قرار دهند و بر حرکت، حافظه و شناخت تأثیر بگذارند.[۱۸۰]
مغز، اگرچه توسط سد خونی - مغزی محافظت میشود، اما میتواند تحت تأثیر عفونتهایی از جمله ویروسها، باکتریها و قارچها قرار گیرد. عفونت ممکن است شامگان (مننژیت)، ماده مغز (آنسفالیت)، یا در داخل ماده مغز (مانند آبسه مغزی) باشد.[۱۸۱] بیماریهای نادر پریون از جمله بیماری کروتزفلد -یاکوب و سویه آن، و کورو نیز ممکن است بر مغز تأثیر بگذارد.[۱۸۱]
تومور مغزی ویرایش
تومورهای مغزی میتوانند خوشخیم یا سرطانی باشند. بیشتر تومورهای بدخیم از قسمت دیگری از بدن، بیشتر از ریه، سینه و پوست بهوجود میآیند. سرطان بافت مغز نیز میتواند رخ دهد و از هر بافت داخل و اطراف مغز منشأ میگیرد. مننژیوما، سرطان مننژهای اطراف مغز، رایجتر از سرطانهای بافت مغزی است. سرطانهای درون مغز ممکن است علائم مربوط به اندازه یا موقعیت خود را ایجاد کنند، با علائمی از جمله سردرد و حالت تهوع، یا گسترش تدریجی نشانههای کانونی مانند مشکل در دیدن تدریجی، خوردن، صحبت کردن یا تغییر خلق و خو همراه است. سرطانها بهطور کلی با استفاده از سیتی اسکن و اسکن امآرآی بررسی میشوند. انواع گوناگونی آزمایش از جمله آزمایش خون و لامبر پانچر ممکن است برای بررسی علت سرطان و ارزیابی نوع و مرحله سرطان مورد استفاده قرار گیرد. کورتیکواستروئید دگزامتازون اغلب برای کاهش تورم بافت مغزی در اطراف تومور تجویز میشود. ممکن است جراحی در نظر گرفته شود، اما با توجه به ماهیت پیچیده بسیاری از تومورها یا بر اساس مرحله یا نوع تومور، پرتودرمانی یا شیمی درمانی مناسب تر تلقی میشود.[۱۸۲]
اختلالات روانی ویرایش
اختلالات روانی مانند افسردگی، روانگسیختگی، اختلال دوقطبی، اختلال استرس پس از سانحه اختلال کمتوجهی - بیشفعالی، اختلال وسواس فکری-عملی، سندرم تورت و اعتیاد، با عملکرد مغز ارتباط دارند.[۱۸۳][۱۸۴] درمان اختلالات روانی ممکن است شامل رواندرمانی، روانپزشکی، مداخله اجتماعی و بازیابی شخصی یا رفتاردرمانی شناختی باشد. مسائل اساسی و پیش آگهیهای مرتبط بین افراد بهطور قابل توجهی متفاوت است.
صرع ویرایش
تصور میشود که تشنجهای صرعی مربوط به فعالیتهای الکتریکی غیرطبیعی است. فعالیت تشنجی میتواند به صورت فقدان هوشیاری، اثرات کانونی مانند حرکت اندام یا موانع گفتاری نمایان گردد، یا ماهیتی کلی داشته باشد. بحران صرعی به تشنج یا مجموعه ای از حملههایی گفته میشود که بیش از ۵ دقیقه ادامه پیدا کند.[۱۸۵] تشنج دلایل زیادی دارد، با این حال بسیاری از تشنجها بدون یافتن علت قطعی رخ میدهند. در افراد مبتلا به صرع، عوامل خطر برای تشنج بیشتر ممکن است شامل بی خوابی، مصرف دارو و الکل و استرس باشد. تشنجها ممکن است با استفاده از آزمایش خون، نوار مغزی یا EEG و تکنیکهای مختلف تصویربرداری پزشکی بر اساس سابقه پزشکی و یافتههای معاینه بالینی ارزیابی شوند. علاوه بر درمان علت زمینه ای و کاهش قرار گرفتن در معرض عوامل خطر، داروهای ضد تشنج میتوانند در جلوگیری از تشنج بیشتر نقش داشته باشند.[۱۸۶]
اختلال مادرزادی ویرایش
برخی از اختلالات مغزی مانند تی-سکس اختلال مادرزادی هستند، و با جهشهای ژنتیکی و کروموزومی مرتبط هستند.[۱۸۷] گروه نادری از اختلالات مادرزادی چون سفالیک که به عنوان لیسنسفالی شناخته میشوند، با فقدان یا ناکافی شدن چین خوردگی قشر مشخص میشود. رشد طبیعی مغز میتواند در دوران بارداری تحت تأثیر کمبودهای تغذیهای، تراتوژنها، بیماریهای عفونی، و استفاده از داروهای تفریحی، از جمله الکل که ممکن است منجر به ناهنجاریهای جنینی ناشی از الکل شود گردد.[۱۸۸]
سکته مغزی ویرایش
سکته مغزی کاهش خون رسانی به ناحیه ای از مغز است که باعث مرگ سلولی و آسیب مغزی میشود. این آسیب میتواند منجر به طیف وسیعی از علائم شود، از جمله علائم «سریع» افتادگی صورت، ضعف بازو و مشکلات گفتاری (از جمله در صحبت کردن و یافتن کلمات یا تشکیل جملات) هستند.[۱۸۹] علائم مربوط به عملکرد ناحیه آسیب دیده مغز است و میتواند به محل و علت احتمالی سکته مغزی اشاره کند. مشکلات حرکتی، گفتاری یا بینایی معمولاً مربوط به مخ است، در حالی که عدم تعادل، دوبینی، سرگیجه و علائم که بر بیش از یک طرف بدن تأثیر میگذارد معمولاً مربوط به ساقه مغز یا مخچه است.[۱۹۰]
بیشتر سکتههای مغزی ناشی از از دست دادن خون است، معمولاً به دلیل آمبولی، پارگی پلاک چربی باعث ایجاد ترومبوز یا تنگ شدن شریانهای کوچک میشود.[۱۹۱] سکته مغزی همچنین میتواند ناشی از خونریزی درون مغز باشد. حملات ایسکمی گذرا (TIAs) سکتههایی هستند که علائم آنها در عرض ۲۴ ساعت برطرف میشود. بررسی سکته مغزی شامل یک معاینه پزشکی (از جمله معاینه عصبی) و گرفتن سابقه پزشکی، با تمرکز بر مدت زمان علائم و عوامل خطر (از جمله فشار خون بالا، فیبریلاسیون دهلیزی و سیگار کشیدن) خواهد بود.[۱۹۲] در بیماران جوانتر نیاز به بررسی بیشتر است. برای تشخیص فیبریلاسیون دهلیزی ممکن است نوار قلب و بیوتل متری انجام شود. سونوگرافی میتواند تنگی سرخرگ کاروتید را بررسی کند. از اکوکاردیوگرام میتوان برای جستجوی لخته در قلب، نارسایی دریچه قلب یا وجود یک نقص دیواره بیندهلیزیتخمدان ثبت شده استفاده کرد. آزمایش خون بهطور معمول به عنوان بخشی از تشخیص پزشکی شامل آزمایش دیابت و مشخصات چربی انجام میشود.[۱۹۳]
برخی از درمانهای سکته مغزی از نظر زمانی بسیار مهم هستند. این موارد شامل انحلال لخته یا برداشتن لخته برای سکتههای ایسکمیک و رفع فشار برای سکتههای خونریزی مغزی است. [۱۹۴][۱۹۵] آنجایی که سکته مغزی از نظر زمانی بسیار مهم است،[۱۹۶] بیمارستانها و حتی مراقبتهای پیش از بیمارستان سکته مغزی شامل تحقیقات سریع است-معمولاً سی تی اسکن برای بررسی سکته مغزی دارای خونریزی و آنژیوگرافی یا سیتی برای ارزیابی شریانهای تأمین کننده مغز استفاده میشود. اسکنهای تصویرسازی تشدید مغناطیسی یا امآرآی، که بهطور گسترده در دسترس نیستند، ممکن است بتوانند ناحیه آسیب دیده مغز را به ویژه در سکته مغزی ایسکمیک با دقت بیشتری نشان دهند.[۱۹۳]
با تجربه سکته مغزی، ممکن است فردی در واحد سکته مغزی بستری شود و درمانها به عنوان پیشگیری از سکتههای مغزی در آینده، از جمله ضد انعقاد مداوم (مانند آسپرین یا کلوپیدوگرل)، داروهای ضد فشار خون بالا و داروهای کاهش دهنده چربی خون، مورد استفاده قرار گیرد. [۱۹۷] یک تیم میانرشتهای شامل آسیب شناسان گفتار، فیزیوتراپیستها، کاردرمانگران و روانشناسان نقش مهمی در حمایت از فرد مبتلا به سکته مغزی و توانبخشی آنها ایفا میکند.[۱۹۸] [۱۹۳] سابقه سکته مغزی خطر ابتلا به زوال عقل را حدود ۷۰ درصد و سکته مغزی جدید خطر را حدود ۱۲۰ افزایش میدهد.[۱۹۹]
مرگ مغزی ویرایش
مرگ مغزی به از بین رفتن کامل عملکرد مغزی اشاره میکند.[۲۰۰][۲۰۱] این آسیب با کما، از دست دادن واکنش غیرارادی و توقف تنفس مشخص میشود،[۲۰۰] با این حال، اعلام مرگ مغزی از نظر جغرافیایی متفاوت است و همیشه پذیرفته نمیشود.[۲۰۱] در برخی کشورها نیز سندرم مرگ ساقه مغز تعریف شدهاست.[۲۰۲] اعلان مرگ مغزی میتواند پیامدهای عمیقی داشته باشد زیرا اعلامیه، بر اساس اصل بیهودگی پزشکی، با قطع حمایت از زندگی همراه خواهد بود و افرادی که دارای مرگ مغزی هستند اغلب دارای اعضای مناسب برای اهداء عضو هستند.[۲۰۱] [۲۰۳] این فرایند اغلب با ارتباط ضعیف با خانواده بیماران مشکلتر میشود.
برای فرد مشکوک به مرگ مغزی تشخیص افتراقی مانند الکترولیت، عصبی و سرکوب شناختی مرتبط با دارو باید حذف شوند.[۲۰۴][۲۰۵] آزمایشهای واکنش غیرارادی و همچنین عدم پاسخ و تنفس میتواند در تصمیمگیری کمک کننده باشد.[۲۰۴] مشاهدات بالینی، از جمله عدم پاسخگویی کامل، یک تشخیص شناخته شده و شواهد تصویربرداری عصبی، ممکن است همه در تصمیمگیری برای مرگ مغزی نقش داشته باشند.[۲۰۰]
تاریخچه ویرایش
دوره باستان ویرایش
پاپیروس ادوین اسمیت[بد]، یک رساله پزشکی[بذ] مصر باستان که در قرن هفدهم پیش از میلاد نوشته شدهاست، حاوی اولین اشاره ثبت شده به مغز است. هیروگلیف برای مغز، که هشت بار در این پاپیروس وجود دارد، نشانهها، تشخیص و پیش آگهی دو آسیب ضربهای به سر را توصیف میکند. پاپیروس سطح خارجی مغز، اثرات آسیب (از جمله تشنج و زبانپریشی)، مننژها و مایع مغزی نخاعی را ذکر میکند.[۲۰۶][۲۰۷]
در قرن پنجم قبل از میلاد، الکمئون در مگنا گراسیا، برای اولین بار مغز را جایگاه ذهن[بر] در نظر گرفت.[۲۰۷] همچنین در قرن پنجم پیش از میلاد در آتن، نویسنده ناشناخته دربارهٔ بیماری مقدس[بز]، یک رساله پزشکی که بخشی از مجموعه بقراط است و بهطور سنتی به بقراط نسبت داده میشود، معتقد بود که مغز مقر هوش است. ارسطو در زیستشناسی خود[بژ] ابتدا قلب را جایگاه هوش میدانست و مغز را مکانیزم خنککننده خون میدانست.[۲۰۸] او استدلال کرد که انسانها از جانوران منطقیتر هستند، زیرا در کنار دلایل دیگر، مغز بزرگتری برای خنک کردن خونگرم خود دارند. ارسطو مننژها را توصیف کرد و بین مخ و مخچه تمایز قائل شد.[۲۰۹]
هروفیلوس از خلقیدون در قرن چهارم و سوم پیش از میلاد، مخ و مخچه را متمایز کرد و اولین توصیف واضح بطنها را ارائه کرد. و با اراسیستراتوس سیئوس روی مغزهای زنده آزمایش کرد. آثار آنها در حال حاضر بیشتر از بین رفتهاست و ما از دستاوردهای آنها بیشتر به دلیل منابع ثانویه اطلاع داریم. برخی از اکتشافات آنها هزاره پس از مرگشان دوباره کشف شد.[۲۱۰] جالینوس پزشک آناتومیست در قرن دوم پس از میلاد، در زمان امپراتوری روم، مغز گوسفند، میمون، سگ و خوک را تشریح کرد. او نتیجه گرفت که از آنجایی که مخچه متراکم تر از مغز است، باید ماهیچهها را کنترل کند، در حالی که مخ نرم است، باید جایی باشد که حواس پردازش شدهاست. جالینوس بیشتر این نظریه را مطرح کرد که مغز با حرکت ارواح حیوانی از طریق بطنها عمل میکند.[۲۱۰][۲۱۱]
دوره رنسانس ویرایش
در سال ۱۳۱۶، موندینو دی لوزی آناتومی[بس] مطالعه مدرن آناتومی مغز در دوران رنسانس را آغاز کرد.[۲۱۲] نیکولو ماسا[بش] در سال ۱۵۳۶ کشف کرد که مغزها با مایع پر شدهاست.[۲۱۳] آرکانجلو پیکولومینی[بص] رومی اولین کسی بود که بین مغز و قشر مخ تمایز قائل شد.[۲۱۴] در سال ۱۵۴۳ آندریاس وسالیوس کتاب هفت جلدی دربارهٔ آناتومی انسان منتشر کرد.[۲۱۴][۲۱۵][۲۱۶] کتاب هفتم مغز و چشم را با تصاویری دقیق از بطنها، اعصاب جمجمهای، غده هیپوفیز، مننژها، ساختارهای چشم، تغذیه عروقی مغز و نخاع و تصویری از اعصاب محیطی پوشش میدهد.[۲۱۷] وسالیوس این باور رایج را که بطنها مسئول عملکرد مغز هستند رد کرد و استدلال کرد که بسیاری از جانوران سامانه بطنی مشابهی با انسان دارند، اما هوش واقعی ندارند.[۲۱۴]
رنه دکارت نظریه ثنویت را برای مقابله با موضوع رابطه مغز با ذهن ارائه کرد. او پیشنهاد کرد که غده صنوبری جایی است که ذهن با بدن در تعامل است، و به عنوان جایگاه روح و به عنوان رابطی است که ارواح جانوران از طریق آن از خون به مغز میرسند.[۲۱۳] این دوگانگی احتمالاً انگیزهای برای آناتومیستهای بعدی فراهم کرد تا رابطه بین جنبههای آناتومیکی و عملکردی آناتومی مغز را بیشتر بررسی کنند.[۲۱۸]
توماس ویلیس را دومین پیشگام در مطالعه عصبشناسی و علوم مغز میدانند. او کتاب کالبدشناسی مغزی[بض] را در سال ۱۶۶۴ نوشت و به دنبال آن آسیبشناسی مغزی در سال ۱۶۶۷ منتشر شد. خونرسانی و توابع پیشنهادی مرتبط با نواحی مختلف مغز آن را مطالعه کرد.[۲۱۴] دایره ویلیس پس از تحقیقات او در مورد خونرسانی به مغز نامگذاری شد و او اولین کسی بود که از کلمه «عصبشناسی» استفاده کرد.[۲۱۹] او توانست مشخص کند قشر فقط از رگهای خونی تشکیل شدهاست، و دیدگاه دو هزاره اخیر که قشر فقط بهطور اتفاقی مهم است.[۲۱۴]
در اواسط قرن نوزدهم، امیل دو بوآ ریموند و هرمان فون هلمهولتز توانستند از یک گالوانومتر برای نشان دادن اینکه تکانههای الکتریکی با سرعت قابل اندازهگیری در امتداد اعصاب عبور میکنند، استفاده کنند و دیدگاه معلم خود یوهانس پیتر مولر مبنی بر اینکه تکانه عصبی یک عملکرد حیاتی و قابل اندازهگیری نبود را رد کردند.[۲۲۰] ریچارد کاتن[بط] در سال ۱۸۷۵ تکانههای الکتریکی را در نیمکره مغزی خرگوشها و میمونها نشان داد.[۲۲۱] در دهه ۱۸۲۰، ژان پیر فلورنس[بظ] پیشگام روش آزمایشی آسیب رساندن به بخشهای خاصی از مغز جانوران بود که اثرات آن بر حرکت و رفتار را توصیف میکرد.[۲۲۲]
دوره مدرن ویرایش
مطالعات مغز با استفاده از میکروسکوپ و توسعه روش رنگ آمیزی بافتی با استفاده از نقره، توسط کامیلو گلگی در دهه ۱۸۸۰ پیچیدهتر شد. این تحقیقات توانست ساختارهای پیچیده نورونهای منفرد را نشان دهد.[۲۲۳] این مورد توسط سانتیاگو رامون کاخال مورد استفاده قرار گرفت و منجر به شکلگیری دکترین نورون[بع] شد، فرضیه انقلابی آن زمان که نورون واحد عملکردی مغز است. او از میکروسکوپ برای کشف بسیاری از انواع سلولها استفاده کرد و عملکردهایی را برای سلولهایی که مشاهده کرد پیشنهاد کرد.[۲۲۳]ب ه همین دلیل، گلجی و کاخال به عنوان بنیانگذاران علوم اعصاب قرن بیستم در نظر گرفته میشوند که هر دو جایزه نوبل را در سال ۱۹۰۶ برای مطالعات و اکتشافات خود در این زمینه به دست آوردند.[۲۲۳]
چارلز شرینگتون کتاب تأثیرگذار خود را در سال ۱۹۰۶ به نام «عمل یکپارچه سیستم عصبی» منتشر کرد که به بررسی عملکرد رفلکسها، رشد تکاملی سیستم عصبی، تخصص عملکردی مغز، و چیدمان و عملکرد سلولی سیستم عصبی مرکزی میپردازد.[۲۲۴] جان فارکور فولتون[بغ]، مجله فیزیولوژی عصبی را تأسیس کرد و اولین کتاب درسی جامع فیزیولوژی سیستم عصبی را در سال ۱۹۳۸ منتشر کرد.[۲۲۵] علوم اعصاب در طول قرن بیستم به عنوان یک رشته دانشگاهی یکپارچه و مشخص شناخته شد. دیوید ریوچ[بف]، فرانسیس او اشمیت[بق] و استفان کوفلر[بک] نقشهای مهمی در ایجاد این رشته ایفا کردند.[۲۲۶] ریوش ادغام تحقیقات پایه تشریحی و فیزیولوژیکی را با روانپزشکی بالینی در مؤسسه تحقیقات ارتش والتر رید آغاز کرد که از دهه ۱۹۵۰ شروع شد.[۲۲۷] در همان دوره، اشمیت برنامه تحقیقاتی علوم اعصاب را تأسیس کرد، یک سازمان بین دانشگاهی و بینالمللی که علوم زیستی، پزشکی، روانشناسی و رفتاری را گرد هم میآورد. خود کلمه عصبشناسی از این برنامه سرچشمه میگیرد.[۲۲۸]
پل بروکا به دنبال کار بر روی بیماران آسیبدیده مغزی، مناطقی از مغز را با عملکردهای خاص، به ویژه زبان در ناحیه بروکا مرتبط کرد.[۲۲۹] جان هالینگز جکسون عملکرد قشر حرکتی را با مشاهده پیشرفت تشنجهای صرع در بدن توصیف کرد. کارل ورنیکه منطقه ای را توصیف کرد که با درک و تولید زبان مرتبط است. کوربینین برادمن[بگ] مناطقی از مغز را بر اساس ظاهر سلولها تقسیم کرد.[۲۲۹] تا سال ۱۹۵۰، شرینگتون، جیمز پاپز[بل] و پال مکلین[بم] بسیاری از عملکردهای ساقه مغز و سیستم لیمبیک را شناسایی کردند.[۲۳۰][۲۳۱] ظرفیت مغز برای سازماندهی مجدد و تغییر با افزایش سن، و یک دوره رشد بحرانی شناخته شده، به نوروپلاستیسیته نسبت داده میشود که توسط مارگارت کنارد[بن]، که در طول دهه ۱۹۳۰–۱۹۴۰ روی میمونها آزمایش کرد، پیشگام بود.[۲۳۲]
هاروی کوشینگ (۱۸۶۹–۱۹۳۹) به عنوان اولین جراح مغز ماهر در جهان شناخته میشود.[۲۳۳] در سال ۱۹۳۷، والتر دندی[بو] عمل جراحی مغز و اعصاب عروقی را با انجام اولین جراحی آنوریسم مغزی آغاز کرد.[۲۳۴]
فلسفه و فرهنگ ویرایش
انسانشناسی-عصبی به مطالعه رابطه بین فرهنگ و مغز میپردازد. به بررسی این موضوع میپردازد که چگونه مغز باعث ایجاد فرهنگ میشود و چگونه فرهنگ بر رشد مغز تأثیر میگذارد.[۲۳۵] تفاوتهای فرهنگی و ارتباط آنها با رشد و ساختار مغز در زمینههای مختلف مورد پژوهش قرار گرفتهاست.[۲۳۶]
ذهن ویرایش
فلسفه ذهن موضوعاتی مانند مشکل درک آگاهی و مشکل ذهن و بدن را مطالعه میکند. رابطه بین مغز و ذهن یک چالش مهم هم از نظر فلسفی و هم از نظر علمی است. این مسئله به دلیل دشواری در توضیح چگونگی اجرای فعالیتهای ذهنی، مانند افکار و احساسات، توسط ساختارهای فیزیکی مانند نورونها و سیناپسها یا هر نوع مکانیسم فیزیکی دیگری است. این مشکل توسط گوتفرید لایب نیتس در قیاس معروف به آسیاب لایبنیتس بیان شد:
انسان موظف است اعتراف کند که ادراک و آنچه وابسته به آن است، بر اساس اصول مکانیکی، یعنی با اشکال و حرکات قابل توضیح نیست. با تصور اینکه ماشینی وجود دارد که ساختش آن را قادر میسازد فکر کند، حس کند و ادراک داشته باشد، میتوان آن را بزرگتر در حالی که همان نسبتها را حفظ کرد، تصور کرد، به طوری که میتوان وارد آن شد، درست مانند یک آسیاب بادی. با فرض این، هنگام بازدید از آن، باید فقط بخشهایی را بیابد که یکدیگر را هل میدهند، و هرگز چیزی را برای توضیح یک ادراک.
— لایب نیتس، مونادولوژی[۲۳۸]
تردید در مورد امکان تبیین مکانیکی اندیشه، رنه دکارت و اکثر فیلسوفان دیگر همراه با او را به سوی دوآلیسم سوق داد: این باور که ذهن تا حدی مستقل از مغز است.[۲۳۹] با این حال، همیشه یک استدلال قوی در جهت مخالف وجود داشتهاست. شواهد تجربی واضحی وجود دارد که نشان میدهد دستکاریهای فیزیکی یا آسیبهای مغزی (بهعنوان مثال توسط داروها یا ضایعات، به ترتیب) میتوانند ذهن را به روشهای قوی و صمیمی تحت تأثیر قرار دهند.[۲۴۰][۲۴۱] در قرن نوزدهم، مورد فینیاس گیج، کارگر راهآهن که توسط میله آهنی محکمی که از مغزش میگذشت مجروح شد، هم محققان و هم مردم را متقاعد کرد که عملکردهای شناختی در مغز متمرکز شدهاند.[۲۳۷] با پیروی از این خط فکری، مجموعه وسیعی از شواهد تجربی برای ارتباط نزدیک بین فعالیت مغز و فعالیت ذهنی، اکثر دانشمندان علوم اعصاب و فیلسوفان معاصر را به مادیگرایی سوق دادهاست و معتقدند که پدیدههای ذهنی در نهایت نتیجه یا قابل تقلیل به پدیدههای فیزیکی هستند.[۲۴۲]
اندازه مغز ویرایش
اندازه مغز و هوش افراد ارتباط قوی با هم ندارند.[۲۴۳] مطالعات تمایل دارند همبستگیهای کوچک تا متوسط (بهطور متوسط حدود ۰٫۳ تا ۰٫۴) بین حجم مغز و IQ را نشان دهند.[۲۴۴] ثابتترین ارتباطها در لوبهای پیشانی، گیجگاهی و آهیانه، هیپوکامپی و مخچه مشاهده میشود، اما اینها تنها مقدار نسبتاً کمی از واریانس در IQ را نشان میدهند، که خود فقط یک رابطه جزئی با هوش عمومی و عملکرد جهانی واقعی دارد.[۲۴۵][۲۴۶]
جانوران دیگر از جمله نهنگها و فیلها مغز بزرگتری نسبت به انسان دارند. با این حال، وقتی نسبت توده مغز به بدن در نظر گرفته شود، مغز انسان تقریباً دو برابر بزرگتر از دلفینهای بینیبطری و سه برابر بزرگتر از یک شامپانزه است. با این حال، نسبت بالا به خودی خود نشاندهنده هوش نیست: جانوران بسیار کوچک نسبت بالایی دارند و حشرهخواران درختی بیشترین ضریب را در بین پستانداران دارد.[۲۴۷]
در فرهنگ عامه ویرایش
عقاید پیشین در مورد اهمیت نسبی اندامهای مختلف بدن انسان، گاهی بر قلب تأکید میکرد.[۲۴۸] در مقابل، تصورات رایج غربی مدرن، تمرکز فزاینده ای را بر مغز معطوف کردهاست.[۲۴۹]
تحقیقات برخی تصورات غلط رایج در مورد مغز را رد کردهاست. این تصورات باستانی و مدرن میشود. این درست نیست (به عنوان مثال) که نورونها بعد از دو سالگی جایگزین نمیشوند. و نه اینکه انسانهای عادی فقط از ده درصد مغز استفاده میکنند.[۲۵۰] فرهنگ عامه نیز با بیان اینکه عملکردها کاملاً مختص یک طرف مغز یا طرف دیگر است، جانبی شدن مغز را بیش از حد ساده کردهاست. آکیو موری اصطلاح «بازی مغز» را برای این تئوری غیرقابل اعتماد ابداع کرد که گذراندن دورههای طولانی بازیهای ویدئویی به ناحیه پیش پیشانی مغز آسیب میرساند و بیان احساسات و خلاقیت را مختل میکند.[۲۵۱]
از نظر تاریخی، بهویژه در اوایل قرن نوزدهم، مغز در فرهنگ عامه از طریق فرنولوژی و شبهعلم که ویژگیهای شخصیتی را به مناطق مختلف قشر مغز اختصاص میداد، نمایان شد. قشر در فرهنگ عامه همچنان مهم است که در کتابها و طنزها پوشش داده شدهاست.[۲۵۲][۲۵۳]
مغز انسان میتواند در داستانهای علمی تخیلی با مضامینی مانند پیوند مغز و سایبورگها (موجودی با ویژگیهایی مانند مغزهای مصنوعی) ظاهر شود.[۲۵۴] کتاب علمی-تخیلی ۱۹۴۲ (که سه بار برای سینما اقتباس شدهاست) مغز دونووان داستان مغزی منزوی را روایت میکند که در شرایط آزمایشگاهی زنده نگه داشته میشود و به تدریج شخصیت قهرمان کتاب را در اختیار میگیرد.[۲۵۵]
کالبدشناسی تطبیقی ویرایش
مغز انسان دارای خواص بسیاری است که در همه مغزهای مهرهداران مشترک است.[۲۵۶] بسیاری از ویژگیهای آن به ویژه قشر مغز شش لایه[۲۵۷] و مجموعهای از ساختارهای مرتبط، از جمله هیپوکامپ و آمیگدال[۲۵۸] در مغز همه پستانداران مشترک است،[۲۵۹] قشر مغز در انسان نسبت به بسیاری از پستانداران دیگر بزرگتر است.[۲۶۰] انسانها نسبت به پستانداران کوچکتر مانند موش صحرایی و گربه، قشر ارتباطی، بخشهای حسی و حرکتی بیشتری دارند.[۲۶۱]
مغز انسان به عنوان مغز پستانداران، قشر مغز بسیار بزرگتری نسبت به اندازه بدن[۲۵۸] و از اکثر پستانداران و یک سیستم بینایی بسیار توسعه یافته دارد.[۲۶۲][۲۶۳] به عنوان یک مغز انسان نما، مغز انسان حتی در مقایسه با مغز یک میمون معمولی بهطور قابل توجهی بزرگ شدهاست.[۲۶۴] توالی تکامل انسان از استرالوپیتکوس (چهار میلیون سال پیش) تا انسان خردمند با افزایش مداوم در اندازه مغز مشخص شد.[۲۶۵][۲۶۶] با افزایش اندازه مغز، این اندازه و شکل جمجمه را تغییر داد، (از حدود ۶۰۰ سانتیمتر مکعب در انسان ماهر به میانگین حدود ۱۵۲۰ سانتیمتر مکعب در نئاندرتال).[۲۶۷] تفاوت در DNA، بیان ژن، و تعاملات ژن-محیط به توضیح تفاوتهای بین عملکرد مغز انسان و سایر نخستیها کمک میکند.[۲۶۸]
یادداشتها ویرایش
- به ویژه حرکت چشمی، عصب قرقرهای (تروکلئار)، عصب سهگانه، عصب ابدکنس، عصب صورت، عصب دهلیزی، عصب گلوفارنکس، عصب واگ، عصب جانبی و عصبهای زیرزبانی.[۲۶۹]
- از جمله رفلکس دهلیزی-چشمی، رفلکس قرنیه، بازتاب تهوع و اتساع مردمکها در پاسخ به نور،[۲۷۰]
- با وجود نقل قولهای گسترده مبنی بر اینکه مغز انسان دارای ۱۰۰ میلیارد نورون و ده برابر یاختههای گلیال است، تعداد مطلق نورونها و سلولهای گلیال در مغز انسان ناشناخته باقی ماندهاست. در اینجا ما این اعداد را با استفاده از تجزیه کننده همسانگرد تعیین میکنیم و آنها را با مقادیر مورد انتظار برای یک پستاندار به اندازه انسان مقایسه میکنیم. ما دریافتیم که مغز انسان بالغ بهطور متوسط دارای ۸۶٫۱ ± ۸٫۱ میلیارد سلول نوین مثبت («نورون») و ۸۴٫۶ ± ۹٫۸ میلیارد سلول نوین منفی («غیر عصبی») است.
- با وجود نقل قولهای گسترده مبنی بر اینکه مغز انسان دارای ۱۰۰ میلیارد نورون و ده برابر سلولهای گلیال است، تعداد مطلق نورونها و سلولهای گلیال در مغز انسان ناشناخته باقی ماندهاست. در اینجا ما این اعداد را با استفاده از تجزیه کننده همسانگرد تعیین میکنیم و آنها را با مقادیر مورد انتظار برای یک پستاندار به اندازه انسان مقایسه میکنیم. ما دریافتیم که مغز انسان بالغ بهطور میانگین دارای ۸۶٫۱ ± ۸٫۱ میلیارد سلول نوین مثبت («نورون») و ۸۴٫۶ ± ۹٫۸ میلیارد سلول نوین منفی («غیر عصبی») است.
واژهنامه ویرایش
- ↑ allocortext
- ↑ association areas، نواحی ارتباطی
- ↑ cerebellar peduncles
- ↑ Claustrum
- ↑ CircumVentricular Organs (CVO)
- ↑ neurotransmission
- ↑ Mind-Body Problem
- ↑ Donovan's Brain
- ↑ Sagittal plane
- ↑ precentral gyrus
- ↑ postcentral gyrus
- ↑ cerebellum، از زبان لاتین به معنای: مغزِ کوچک
- ↑ glia limitans
- ↑ longitudinal fissure
- ↑ petalia
- ↑ gyrus
- ↑ sulcus
- ↑ Brodmann's areas
- ↑ association areas
- ↑ septum pellucidum
- ↑ nucleus accumbens
- ↑ olfactory tubercle
- ↑ basal forebrain
- ↑ nucleus basalis
- ↑ diagonal band of Broca
- ↑ substantia innominata
- ↑ flocculondular lobe
- ↑ cerebellar peduncles
- ↑ neural stem cells
- ↑ Bergmann glia
- ↑ tanycytes
- ↑ stellate cells
- ↑ glia limitans
- ↑ neuroimmune system
- ↑ effector cell
- ↑ ELAV-like protein 3
- ↑ Neurogranin
- ↑ Receptor expression-enhancing protein 2
- ↑ Glial fibrillary acidic protein
- ↑ S100 calcium-binding protein B
- ↑ Oligodendrocyte transcription factor
- ↑ Subarachnoid cisterns
- ↑ meningeal lymphatic vessels
- ↑ carotid canal
- ↑ cavernous sinus
- ↑ Cerebral veins
- ↑ Great cerebral vein
- ↑ Superior_sagittal_sinus
- ↑ Straight_sinus
- ↑ Pericytes
- ↑ circumventricular organs
- ↑ Motor cortex
- ↑ Precentral gyrus
- ↑ premotor area
- ↑ Supplementary motor area
- ↑ Corticospinal tract
- ↑ Medullary pyramids
- ↑ motor homunculus
- ↑ Ventrobasal complex
- ↑ Spinothalamic tract
- ↑ Pneumotaxic centre
- ↑ Decade of the Brain
- ↑ Cortical stimulation mapping
- ↑ Single-unit recordings
- ↑ Haemodynamic response
- ↑ Brain morphometry
- ↑ Axon terminal
- ↑ Salience network
- ↑ Default mode network
- ↑ Glymphatic system
- ↑ Diffuse_axonal_injury
- ↑ Skull_fracture
- ↑ Coup_contrecoup_injury
- ↑ Edwin Smith Papyrus
- ↑ Medical_literature
- ↑ Sensorium
- ↑ On the Sacred Disease
- ↑ Aristotle's biology
- ↑ Mondino de Luzzi's Anathomia
- ↑ Niccolò Massa
- ↑ Arcangelo Piccolomini
- ↑ Anatomy of the brain
- ↑ Richard Caton
- ↑ Jean Pierre Flourens
- ↑ Neuron doctrine
- ↑ John Farquhar Fulton
- ↑ David Rioch
- ↑ Francis O. Schmitt
- ↑ Stephen Kuffler
- ↑ Korbinian Brodmann
- ↑ James Papez
- ↑ Paul D. MacLean
- ↑ Margaret Kennard
- ↑ Walter Dandy
جستارهای وابسته ویرایش
منابع ویرایش
- ↑ "Cerebrum Etymology". dictionary.com. Archived from the original on October 24, 2015. Retrieved October 24, 2015.
- ↑ "Encephalo- Etymology". واژهنامه برخط ریشهشناسی. Archived from the original on October 2, 2017. Retrieved October 24, 2015.
- ↑ Fan, Xue; Markram, Henry (2019-05-07). "A Brief History of Simulation Neuroscience". Frontiers in Neuroinformatics. 13: 32. doi:10.3389/fninf.2019.00032. ISSN 1662-5196. PMC 6513977. PMID 31133838.
- ↑ Parent, A.; Carpenter, M.B. (1995). "Ch. 1". Carpenter's Human Neuroanatomy. Williams & Wilkins. ISBN 978-0-683-06752-1.
- ↑ Bigos, K.L.; Hariri, A.; Weinberger, D. (2015). Neuroimaging Genetics: Principles and Practices. Oxford University Press. p. 157. ISBN 978-0-19-992022-8.
- ↑ ۶٫۰ ۶٫۱ Cosgrove, K.P.; Mazure, C.M.; Staley, J.K. (2007). "Evolving knowledge of sex differences in brain structure, function, and chemistry". Biol Psychiatry. 62 (8): 847–855. doi:10.1016/j.biopsych.2007.03.001. PMC 2711771. PMID 17544382.
- ↑ Molina, D. Kimberley; DiMaio, Vincent J.M. (2012). "Normal Organ Weights in Men". The American Journal of Forensic Medicine and Pathology. 33 (4): 368–372. doi:10.1097/PAF.0b013e31823d29ad. ISSN 0195-7910. PMID 22182984. S2CID 32174574.
- ↑ Molina, D. Kimberley; DiMaio, Vincent J. M. (2015). "Normal Organ Weights in Women". The American Journal of Forensic Medicine and Pathology. 36 (3): 182–187. doi:10.1097/PAF.0000000000000175. ISSN 0195-7910. PMID 26108038. S2CID 25319215.
- ↑ ۹٫۰ ۹٫۱ ۹٫۲ ۹٫۳ ۹٫۴ Gray's Anatomy 2008, pp. 227–9.
- ↑ ۱۰٫۰ ۱۰٫۱ Gray's Anatomy 2008, pp. 335–7.
- ↑ ۱۱٫۰ ۱۱٫۱ Ribas, G. C. (2010). "The cerebral sulci and gyri". Neurosurgical Focus. 28 (2): 7. doi:10.3171/2009.11.FOCUS09245. PMID 20121437.
- ↑ Frigeri, T.; Paglioli, E.; De Oliveira, E.; Rhoton Jr, A. L. (2015). "Microsurgical anatomy of the central lobe". Journal of Neurosurgery. 122 (3): 483–98. doi:10.3171/2014.11.JNS14315. PMID 25555079.
- ↑ Purves 2012, p. 724.
- ↑ Cipolla, M.J. (January 1, 2009). Anatomy and Ultrastructure. Morgan & Claypool Life Sciences. Archived from the original on October 1, 2017.
- ↑ "A Surgeon's-Eye View of the Brain". NPR.org. Archived from the original on November 7, 2017.
- ↑ Sampaio-Baptista, C; Johansen-Berg, H (December 20, 2017). "White Matter Plasticity in the Adult Brain". Neuron. 96 (6): 1239–1251. doi:10.1016/j.neuron.2017.11.026. PMC 5766826. PMID 29268094.
- ↑ Davey, G. (2011). Applied Psychology. John Wiley & Sons. p. 153. ISBN 978-1-4443-3121-9.
- ↑ Arsava, E. Y.; Arsava, E. M.; Oguz, K. K.; Topcuoglu, M. A. (2019). "Occipital petalia as a predictive imaging sign for transverse sinus dominance". Neurological Research. 41 (4): 306–311. doi:10.1080/01616412.2018.1560643. PMID 30601110. S2CID 58546404.
- ↑ Ackerman, S. (1992). Discovering the brain. Washington, D.C.: National Academy Press. pp. 22–25. ISBN 978-0-309-04529-2.
- ↑ Larsen 2001, pp. 455–456.
- ↑ Kandel, E.R.; Schwartz, J.H.; Jessel T.M. (2000). Principles of Neural Science. McGraw-Hill Professional. p. 324. ISBN 978-0-8385-7701-1.
- ↑ Guyton & Hall 2011, p. 574.
- ↑ Guyton & Hall 2011, p. 667.
- ↑ Principles of Anatomy and Physiology 12th Edition – Tortora, p. 519.
- ↑ ۲۵٫۰ ۲۵٫۱ ۲۵٫۲ Freberg, L. (2009). Discovering Biological Psychology. Cengage Learning. pp. 44–46. ISBN 978-0-547-17779-3.
- ↑ ۲۶٫۰ ۲۶٫۱ Kolb, B.; Whishaw, I. (2009). Fundamentals of Human Neuropsychology. Macmillan. pp. 73–75. ISBN 978-0-7167-9586-5.
- ↑ ۲۷٫۰ ۲۷٫۱ Haldane, Morgan; Cunningham, Giles; Androutsos, Chris; Frangou, Sophia (March 2008). "Structural brain correlates of response inhibition in Bipolar Disorder I". Journal of Psychopharmacology (Oxford, England). 22 (2): 138–143. doi:10.1177/0269881107082955. ISSN 0269-8811. PMID 18308812.
- ↑ Pocock 2006, p. 64.
- ↑ ۲۹٫۰ ۲۹٫۱ Purves 2012, p. 399.
- ↑ Gray's Anatomy 2008, pp. 325–6.
- ↑ Goll, Y.; Atlan, G.; Citri, A. (August 2015). "Attention: the claustrum". Trends in Neurosciences. 38 (8): 486–95. doi:10.1016/j.tins.2015.05.006. PMID 26116988. S2CID 38353825.
- ↑ Goard, M.; Dan, Y. (October 4, 2009). "Basal forebrain activation enhances cortical coding of natural scenes". Nature Neuroscience. 12 (11): 1444–1449. doi:10.1038/nn.2402. PMC 3576925. PMID 19801988.
- ↑ Guyton & Hall 2011, p. 699.
- ↑ ۳۴٫۰ ۳۴٫۱ ۳۴٫۲ Gray's Anatomy 2008, p. 298.
- ↑ Netter, F. (2014). Atlas of Human Anatomy Including Student Consult Interactive Ancillaries and Guides (6th ed.). Philadelphia, Penn.: W B Saunders Co. p. 114. ISBN 978-1-4557-0418-7.
- ↑ ۳۶٫۰ ۳۶٫۱ Gray's Anatomy 2008, p. 297.
- ↑ Guyton & Hall 2011, pp. 698–9.
- ↑ Squire 2013, pp. 761–763.
- ↑ ۳۹٫۰۰ ۳۹٫۰۱ ۳۹٫۰۲ ۳۹٫۰۳ ۳۹٫۰۴ ۳۹٫۰۵ ۳۹٫۰۶ ۳۹٫۰۷ ۳۹٫۰۸ ۳۹٫۰۹ ۳۹٫۱۰ ۳۹٫۱۱ ۳۹٫۱۲ ۳۹٫۱۳ ۳۹٫۱۴ ۳۹٫۱۵ ۳۹٫۱۶ ۳۹٫۱۷ ۳۹٫۱۸ ۳۹٫۱۹ ۳۹٫۲۰ ۳۹٫۲۱ Gray's Anatomy 2008.
- ↑ ۴۰٫۰ ۴۰٫۱ ۴۰٫۲ ۴۰٫۳ ۴۰٫۴ ۴۰٫۵ Guyton & Hall 2011.
- ↑ ۴۱٫۰ ۴۱٫۱ ۴۱٫۲ ۴۱٫۳ Purves 2012.
- ↑ ۴۲٫۰ ۴۲٫۱ ۴۲٫۲ ۴۲٫۳ Azevedo, Frederico A. C.; Carvalho, Ludmila R. B.; Grinberg, Lea T.; Farfel, José Marcelo; Ferretti, Renata E. L.; Leite, Renata E. P.; Jacob Filho, Wilson; Lent, Roberto; Herculano-Houzel, Suzana (2009-04-10). "Equal numbers of neuronal and nonneuronal cells make the human brain an isometrically scaled-up primate brain". The Journal of Comparative Neurology. 513 (5): 532–541. doi:10.1002/cne.21974. ISSN 1096-9861. PMID 19226510.
- ↑ ۴۳٫۰ ۴۳٫۱ ۴۳٫۲ ۴۳٫۳ Polyzoidis, S.; Koletsa, T.; Panagiotidou, S.; Ashkan, K.; Theoharides, T.C. (2015). "Mast cells in meningiomas and brain inflammation". Journal of Neuroinflammation. 12 (1): 170. doi:10.1186/s12974-015-0388-3. PMC 4573939. PMID 26377554.
- ↑ Budzyński, J; Kłopocka, M. (2014). "Brain-gut axis in the pathogenesis of Helicobacter pylori infection". World J. Gastroenterol. 20 (18): 5212–25. doi:10.3748/wjg.v20.i18.5212. PMC 4017036. PMID 24833851.
- ↑ Carabotti, M.; Scirocco, A.; Maselli, M.A.; Severi, C. (2015). "The gut-brain axis: interactions between enteric microbiota, central and enteric nervous systems". Ann Gastroenterol. 28 (2): 203–209. PMC 4367209. PMID 25830558.
- ↑ Sjöstedt, Evelina; Fagerberg, Linn; Hallström, Björn M.; Häggmark, Anna; Mitsios, Nicholas; Nilsson, Peter; Pontén, Fredrik; Hökfelt, Tomas; Uhlén, Mathias (June 15, 2015). "Defining the human brain proteome using transcriptomics and antibody-based profiling with a focus on the cerebral cortex". PLOS ONE. 10 (6): e0130028. Bibcode:2015PLoSO..1030028S. doi:10.1371/journal.pone.0130028. ISSN 1932-6203. PMC 4468152. PMID 26076492.
- ↑ Iliff, JJ; Nedergaard, M (June 2013). "Is there a cerebral lymphatic system?". Stroke. 44 (6 Suppl 1): S93-5. doi:10.1161/STROKEAHA.112.678698. PMC 3699410. PMID 23709744.
- ↑ Gaillard, F. "Glymphatic pathway". radiopaedia.org. Archived from the original on October 30, 2017.
- ↑ ۴۹٫۰ ۴۹٫۱ ۴۹٫۲ Bacyinski, Andrew; Xu, Maosheng; Wang, Wei; Hu, Jiani (2017). "The Paravascular Pathway for Brain Waste Clearance: Current Understanding, Significance and Controversy". Frontiers in Neuroanatomy. 11: 101. doi:10.3389/fnana.2017.00101. ISSN 1662-5129. PMC 5681909. PMID 29163074.
- ↑ Dissing-Olesen, L.; Hong, S.; Stevens, B. (August 2015). "New brain lymphatic vessels drain old concepts". EBioMedicine. 2 (8): 776–7. doi:10.1016/j.ebiom.2015.08.019. PMC 4563157. PMID 26425672.
- ↑ ۵۱٫۰ ۵۱٫۱ Sun, BL; Wang, LH; Yang, T; Sun, JY; Mao, LL; Yang, MF; Yuan, H; Colvin, RA; Yang, XY (April 2018). "Lymphatic drainage system of the brain: A novel target for intervention of neurological diseases". Progress in Neurobiology. 163–164: 118–143. doi:10.1016/j.pneurobio.2017.08.007. PMID 28903061.
- ↑ ۵۲٫۰ ۵۲٫۱ ۵۲٫۲ ۵۲٫۳ ۵۲٫۴ Elsevier's 2007.
- ↑ Daneman, R.; Zhou, L.; Kebede, A.A.; Barres, B.A. (November 25, 2010). "Pericytes are required for blood-brain barrier integrity during embryogenesis". Nature. 468 (7323): 562–6. Bibcode:2010Natur.468..562D. doi:10.1038/nature09513. PMC 3241506. PMID 20944625.
- ↑ Sadler, T. (2010). Langman's medical embryology (11th ed.). Philadelphia: Lippincott Williams & Wilkins. p. 293. ISBN 978-0-7817-9069-7.
- ↑ ۵۵٫۰ ۵۵٫۱ Larsen 2001, p. 419.
- ↑ ۵۶٫۰ ۵۶٫۱ ۵۶٫۲ Larsen 2001, pp. 85–88.
- ↑ Purves 2012, pp. 480–482.
- ↑ ۵۸٫۰ ۵۸٫۱ ۵۸٫۲ ۵۸٫۳ Larsen 2001, pp. 445–446.
- ↑ "OpenStax CNX". cnx.org. Archived from the original on May 5, 2015. Retrieved May 5, 2015.
- ↑ Larsen 2001, pp. 85–87.
- ↑ Purves 2012, pp. 481–484.
- ↑ Purves, Dale; Augustine, George J; Fitzpatrick, David; Katz, Lawrence C; LaMantia, Anthony-Samuel; McNamara, James O; Williams, S Mark, eds. (2001). "Rhombomeres". Neuroscience (2nd ed.). ISBN 978-0-87893-742-4.
- ↑ Chen, X. (2012). Mechanical Self-Assembly: Science and Applications. Springer Science & Business Media. pp. 188–189. ISBN 978-1-4614-4562-3.
- ↑ Chen, X. (2012). Mechanical Self-Assembly: Science and Applications. Springer Science & Business Media. pp. 188–189. ISBN 978-1-4614-4562-3.
- ↑ Ronan, L; Voets, N; Rua, C; Alexander-Bloch, A; Hough, M; Mackay, C; Crow, TJ; James, A; Giedd, JN; Fletcher, PC (August 2014). "Differential tangential expansion as a mechanism for cortical gyrification". Cerebral Cortex. 24 (8): 2219–28. doi:10.1093/cercor/bht082. PMC 4089386. PMID 23542881.
- ↑ Ackerman, S. (1992). Discovering the brain. Washington, D.C.: National Academy Press. pp. 22–25. ISBN 978-0-309-04529-2.
- ↑ Van Essen, DC (January 23, 1997). "A tension-based theory of morphogenesis and compact wiring in the central nervous system". Nature. 385 (6614): 313–8. Bibcode:1997Natur.385..313E. doi:10.1038/385313a0. PMID 9002514. S2CID 4355025.
- ↑ Ronan, L; Voets, N; Rua, C; Alexander-Bloch, A; Hough, M; Mackay, C; Crow, TJ; James, A; Giedd, JN; Fletcher, PC (August 2014). "Differential tangential expansion as a mechanism for cortical gyrification". Cerebral Cortex. 24 (8): 2219–28. doi:10.1093/cercor/bht082. PMC 4089386. PMID 23542881.
- ↑ Ronan, L; Voets, N; Rua, C; Alexander-Bloch, A; Hough, M; Mackay, C; Crow, TJ; James, A; Giedd, JN; Fletcher, PC (August 2014). "Differential tangential expansion as a mechanism for cortical gyrification". Cerebral Cortex. 24 (8): 2219–28. doi:10.1093/cercor/bht082. PMC 4089386. PMID 23542881.
- ↑ Borrell, V (24 January 2018). "How Cells Fold the Cerebral Cortex". The Journal of Neuroscience. 38 (4): 776–783. doi:10.1523/JNEUROSCI.1106-17.2017. PMC 6596235. PMID 29367288.
- ↑ Florio, M.; et al. (March 27, 2015). "Human-specific gene ARHGAP11B promotes basal progenitor amplification and neocortex expansion". Science. 347 (6229): 1465–70. Bibcode:2015Sci...347.1465F. doi:10.1126/science.aaa1975. PMID 25721503. S2CID 34506325.
- ↑ "Brain Anatomy and How the Brain Works". www.hopkinsmedicine.org (به انگلیسی). Retrieved 2021-10-18.
- ↑ انجمن علوم اعصاب، مترجم رضا پناهی. بهنام سور، علی شهبازی، عباس حقپرست، حقایق مغز. تهران: مؤسسه انتشارات ستایش هستی، ۱۳۹۸ شابک ۹۷۸−۶۲۲−۶۴۴۵−۶۳−۴، ص ۱۱.
- ↑ «Brain anatomy, Anatomy of the human brain | Mayfield Brain & Spine Cincinnati, Ohio». mayfieldclinic.com (به انگلیسی). دریافتشده در ۲۰۲۱-۱۰-۱۸.
- ↑ «Parts of the Brain | Introduction to Psychology». courses.lumenlearning.com (به انگلیسی). دریافتشده در ۲۰۲۱-۱۰-۱۸.
- ↑ انجمن علوم اعصاب، مترجم رضا پناهی. بهنام سور، علی شهبازی، عباس حقپرست، حقایق مغز. تهران: مؤسسه انتشارات ستایش هستی، ۱۳۹۸ شابک ۹۷۸−۶۲۲−۶۴۴۵−۶۳−۴، ص ۸۱.
- ↑ Guyton & Hall 2011, p. 685.
- ↑ Guyton & Hall 2011, p. 687.
- ↑ ۷۹٫۰ ۷۹٫۱ Guyton & Hall 2011, p. 686.
- ↑ Genc, Baris; Gozutok, Oge; Ozdinler, P. Hande (2019-08-07). "Complexity of Generating Mouse Models to Study the Upper Motor Neurons: Let Us Shift Focus from Mice to Neurons". International Journal of Molecular Sciences. 20 (16): E3848. doi:10.3390/ijms20163848. ISSN 1422-0067. PMC 6720674. PMID 31394733.
- ↑ Marieb, E.; Hoehn, K. (2007). Human Anatomy and Physiology (7th ed.). Pearson Benjamin Cummings. ISBN 978-0-8053-5909-1.
- ↑ Guyton & Hall 2011, pp. 698, 708.
- ↑ Diaz, Eric; Morales, Humberto (October 2016). "Spinal Cord Anatomy and Clinical Syndromes". Seminars in ultrasound, CT, and MR. 37 (5): 360–371. doi:10.1053/j.sult.2016.05.002. ISSN 1558-5034. PMID 27616310.
- ↑ ۸۴٫۰ ۸۴٫۱ Hellier, J. (2014). The Brain, the Nervous System, and Their Diseases [3 volumes]. ABC-CLIO. pp. 300–303. ISBN 978-1-61069-338-7.
- ↑ ۸۵٫۰ ۸۵٫۱ Guyton & Hall 2011, pp. 571–576.
- ↑ Guyton & Hall 2011, pp. 573–574.
- ↑ Guyton & Hall 2011, pp. 623–631.
- ↑ Guyton & Hall 2011, pp. 739–740.
- ↑ Pocock 2006, pp. 138–139.
- ↑ Squire 2013, pp. 525–526.
- ↑ Guyton & Hall 2011, pp. 647–648.
- ↑ ۹۲٫۰ ۹۲٫۱ Guyton & Hall 2011, pp. 202–203.
- ↑ Guyton & Hall 2011, pp. 205–208.
- ↑ ۹۴٫۰ ۹۴٫۱ ۹۴٫۲ ۹۴٫۳ Guyton & Hall 2011, pp. 505–509.
- ↑ "Brain Basics: Understanding Sleep | National Institute of Neurological Disorders and Stroke". www.ninds.nih.gov. Archived from the original on December 22, 2017.
- ↑ Guyton & Hall 2011, p. 723.
- ↑ Davis, J.F.; Choi, D.L.; Benoit, S.C. (2011). "24. Orexigenic Hypothalamic Peptides Behavior and Feeding – 24.5 Orexin". In Preedy, V.R.; Watson, R.R.; Martin, C.R. (eds.). Handbook of Behavior, Food and Nutrition. Springer. pp. 361–362. ISBN 978-0-387-92271-3.
- ↑ Squire 2013, p. 800.
- ↑ Squire 2013, p. 803.
- ↑ Squire 2013, p. 805.
- ↑ Guyton & Hall 2011, pp. 720–2.
- ↑ Poeppel, D.; Emmorey, K.; Hickok, G.; Pylkkänen, L. (October 10, 2012). "Towards a new neurobiology of language". The Journal of Neuroscience. 32 (41): 14125–14131. doi:10.1523/JNEUROSCI.3244-12.2012. PMC 3495005. PMID 23055482.
- ↑ Hickok, Gregory (September 2009). "The functional neuroanatomy of language". Physics of Life Reviews. 6 (3): 121–143. doi:10.1016/j.plrev.2009.06.001. ISSN 1873-1457. PMC 2747108. PMID 20161054.
- ↑ Fedorenko, E.; Kanwisher, N. (2009). "Neuroimaging of language: why hasn't a clearer picture emerged?". Language and Linguistics Compass. 3 (4): 839–865. doi:10.1111/j.1749-818x.2009.00143.x. S2CID 2833893.
- ↑ Damasio, H. (2001). "Neural basis of language disorders". In Chapey, Roberta (ed.). Language intervention strategies in aphasia and related neurogenic communication disorders (4th ed.). Lippincott Williams & Wilkins. pp. 18–36. ISBN 978-0-7817-2133-2. OCLC 45952164.
- ↑ ۱۰۶٫۰ ۱۰۶٫۱ Berntson, G.; Cacioppo, J. (2009). Handbook of Neuroscience for the Behavioral Sciences, Volume 1. John Wiley & Sons. p. 145. ISBN 978-0-470-08355-0.
- ↑ Hellier, J. (2014). The Brain, the Nervous System, and Their Diseases [3 volumes]. ABC-CLIO. p. 1135. ISBN 978-1-61069-338-7.
- ↑ Kolb, B.; Whishaw, I.Q. (2013). Introduction to Brain and Behavior. Macmillan Higher Education. p. 296. ISBN 978-1-4641-3960-4.
- ↑ Sherwood, L. (2012). Human Physiology: From Cells to Systems. Cengage Learning. p. 181. ISBN 978-1-133-70853-7.
- ↑ Kalat, J (2015). Biological Psychology. Cengage Learning. p. 425. ISBN 978-1-305-46529-9.
- ↑ ۱۱۱٫۰ ۱۱۱٫۱ Cowin, S.C.; Doty, S.B. (2007). Tissue Mechanics. Springer Science & Business Media. p. 4. ISBN 978-0-387-49985-7.
- ↑ Morris, C.G.; Maisto, A.A. (2011). Understanding Psychology. Prentice Hall. p. 56. ISBN 978-0-205-76906-3.
- ↑ Morris, C.G.; Maisto, A.A. (2011). Understanding Psychology. Prentice Hall. p. 56. ISBN 978-0-205-76906-3.
- ↑ Kolb, B.; Whishaw, I.Q. (2013). Introduction to Brain and Behavior (Loose-Leaf). Macmillan Higher Education. pp. 524–549. ISBN 978-1-4641-3960-4.
- ↑ Kolb, B.; Whishaw, I.Q. (2013). Introduction to Brain and Behavior (Loose-Leaf). Macmillan Higher Education. pp. 524–549. ISBN 978-1-4641-3960-4.
- ↑ Schacter, D.L.; Gilbert, D.T.; Wegner, D.M. (2009). Introducing Psychology. Macmillan. p. 80. ISBN 978-1-4292-1821-4.
- ↑ Sander, David (2013). Armony, J.; Vuilleumier, Patrik (eds.). The Cambridge handbook of human affective neuroscience. Cambridge: Cambridge Univ. Press. p. 16. ISBN 978-0-521-17155-7.
- ↑ Lindquist, KA.; Wager, TD.; Kober, H; Bliss-Moreau, E; Barrett, LF (May 23, 2012). "The brain basis of emotion: A meta-analytic review". Behavioral and Brain Sciences. 35 (3): 121–143. doi:10.1017/S0140525X11000446. PMC 4329228. PMID 22617651.
- ↑ Phan, K. Luan; Wager, Tor; Taylor, Stephan F.; Liberzon, Israel (June 2002). "Functional neuroanatomy of emotion: a meta-analysis of emotion activation studies in PET and fMRI". NeuroImage. 16 (2): 331–348. doi:10.1006/nimg.2002.1087. ISSN 1053-8119. PMID 12030820.
- ↑ Malenka, RC; Nestler, EJ; Hyman, SE (2009). "Preface". In Sydor, A; Brown, RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. p. xiii. ISBN 978-0-07-148127-4.
- ↑ Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Chapter 14: Higher Cognitive Function and Behavioral Control". Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (3rd ed.). New York: McGraw-Hill Medical. ISBN 978-0-07-182770-6.
- ↑ ۱۲۲٫۰ ۱۲۲٫۱ ۱۲۲٫۲ Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Chapter 14: Higher Cognitive Function and Behavioral Control". Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (3rd ed.). New York: McGraw-Hill Medical. ISBN 978-0-07-182770-6.
- ↑ ۱۲۳٫۰ ۱۲۳٫۱ Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin". Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (3rd ed.). New York: McGraw-Hill Medical. ISBN 978-0-07-182770-6.
- ↑ ۱۲۴٫۰ ۱۲۴٫۱ ۱۲۴٫۲ ۱۲۴٫۳ ۱۲۴٫۴ Diamond, A (2013). "Executive functions". Annual Review of Psychology. 64: 135–168. doi:10.1146/annurev-psych-113011-143750. PMC 4084861. PMID 23020641.Figure 4: Executive functions and related terms بایگانیشده در مه ۹, ۲۰۱۸ توسط Wayback Machine
- ↑ ۱۲۵٫۰ ۱۲۵٫۱ ۱۲۵٫۲ ۱۲۵٫۳ Hyun, J.C.; Weyandt, L.L.; Swentosky, A. (2014). "Chapter 2: The Physiology of Executive Functioning". In Goldstein, S.; Naglieri, J. (eds.). Handbook of Executive Functioning. New York: Springer. pp. 13–23. ISBN 978-1-4614-8106-5.
- ↑ Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Chapter 14: Higher Cognitive Function and Behavioral Control". Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (3rd ed.). New York: McGraw-Hill Medical. ISBN 978-0-07-182770-6.
- ↑ ۱۲۷٫۰ ۱۲۷٫۱ Van Essen, D. C.; Ugurbil, K.; Auerbach, E.; Barch, D.; Behrens, T. E. J.; Bucholz, R.; Chang, A.; Chen, L.; Corbetta, M. (2012-10-01). "The Human Connectome Project: a data acquisition perspective". NeuroImage. 62 (4): 2222–2231. doi:10.1016/j.neuroimage.2012.02.018. ISSN 1095-9572. PMC 3606888. PMID 22366334.
- ↑ Tanner, Kimberly D. (2006-01-01). "Issues in Neuroscience Education: Making Connections". CBE: Life Sciences Education. 5 (2): 85. doi:10.1187/cbe.06-04-0156. ISSN 1931-7913. PMC 1618510.
- ↑ Shulman, Robert G. (2013). "Neuroscience: A Multidisciplinary, Multilevel Field". Brain Imaging: What it Can (and Cannot) Tell Us About Consciousness. Oxford University Press. p. 59. ISBN 978-0-19-983872-1.
- ↑ Jones, E.G.; Mendell, L.M. (April 30, 1999). "Assessing the Decade of the Brain". Science. 284 (5415): 739. Bibcode:1999Sci...284..739J. doi:10.1126/science.284.5415.739. PMID 10336393.
- ↑ "A $4.5 Billion Price Tag for the BRAIN Initiative?". Science | AAAS. June 5, 2014. Archived from the original on June 18, 2017.
- ↑ Towle, V.L.; et al. (January 1993). "The spatial location of EEG electrodes: locating the best-fitting sphere relative to cortical anatomy". Electroencephalography and Clinical Neurophysiology. 86 (1): 1–6. doi:10.1016/0013-4694(93)90061-y. PMID 7678386.
- ↑ Silverstein, J. (2012). "Mapping the Motor and Sensory Cortices: A Historical Look and a Current Case Study in Sensorimotor Localization and Direct Cortical Motor Stimulation". The Neurodiagnostic Journal. 52 (1): 54–68. PMID 22558647. Archived from the original on November 17, 2012.
- ↑ Boraud, T.; Bezard, E.; et al. (2002). "From single extracellular unit recording in experimental and human Parkinsonism to the development of a functional concept of the role played by the basal ganglia in motor control". Progress in Neurobiology. 66 (4): 265–283. doi:10.1016/s0301-0082(01)00033-8. PMID 11960681.
- ↑ Lancaster, MA; Renner, M; Martin, CA; Wenzel, D; Bicknell, LS; Hurles, ME; Homfray, T; Penninger, JM; Jackson, AP (September 19, 2013). "Cerebral organoids model human brain development and microcephaly". Nature. 501 (7467): 373–9. Bibcode:2013Natur.501..373L. doi:10.1038/nature12517. PMC 3817409. PMID 23995685.
- ↑ Lee, CT; Bendriem, RM; Wu, WW; Shen, RF (August 20, 2017). "3D brain Organoids derived from pluripotent stem cells: promising experimental models for brain development and neurodegenerative disorders". Journal of Biomedical Science. 24 (1): 59. doi:10.1186/s12929-017-0362-8. PMC 5563385. PMID 28822354.
- ↑ "Magnetic Resonance, a critical peer-reviewed introduction; functional MRI". European Magnetic Resonance Forum. Archived from the original on June 2, 2017. Retrieved June 30, 2017.
- ↑ Buxton, R.; Uludag, K.; Liu, T. (2004). "Modeling the haemodynamic response to brain activation". NeuroImage. 23: S220–S233. CiteSeerX 10.1.1.329.29. doi:10.1016/j.neuroimage.2004.07.013. PMID 15501093.
- ↑ ۱۳۹٫۰ ۱۳۹٫۱ Irimia, Andrei; Chambers, Micah C.; Torgerson, Carinna M.; Van Horn, John D. (2012-04-02). "Circular representation of human cortical networks for subject and population-level connectomic visualization". NeuroImage. 60 (2): 1340–1351. doi:10.1016/j.neuroimage.2012.01.107. ISSN 1095-9572. PMC 3594415. PMID 22305988.
- ↑ Biswal, Bharat B. (2012-08-15). "Resting state fMRI: a personal history". NeuroImage. 62 (2): 938–944. doi:10.1016/j.neuroimage.2012.01.090. ISSN 1095-9572. PMID 22326802.
- ↑ Basser, P. J.; Pajevic, S.; Pierpaoli, C.; Duda, J.; Aldroubi, A. (October 2000). "In vivo fiber tractography using DT-MRI data". Magnetic Resonance in Medicine. 44 (4): 625–632. doi:10.1002/1522-2594(200010)44:4<625::aid-mrm17>3.0.co;2-o. ISSN 0740-3194. PMID 11025519.
- ↑ Lepage, M. (2010). "Research at the Brain Imaging Centre". Douglas Mental Health University Institute. Archived from the original on March 5, 2012.
- ↑ Sim, Adelene Y. L.; Minary, Peter; Levitt, Michael (June 2012). "Modeling nucleic acids". Current Opinion in Structural Biology. 22 (3): 273–278. doi:10.1016/j.sbi.2012.03.012. ISSN 1879-033X. PMC 4028509. PMID 22538125.
- ↑ Saidijam, Massoud; Karimi Dermani, Fatemeh; Sohrabi, Sareh; Patching, Simon G. (May 2018). "Efflux proteins at the blood-brain barrier: review and bioinformatics analysis". Xenobiotica; the Fate of Foreign Compounds in Biological Systems. 48 (5): 506–532. doi:10.1080/00498254.2017.1328148. ISSN 1366-5928. PMID 28481715.
- ↑ ۱۴۵٫۰ ۱۴۵٫۱ Steward, Charles A.; Parker, Alasdair P. J.; Minassian, Berge A.; Sisodiya, Sanjay M.; Frankish, Adam; Harrow, Jennifer (2017-05-30). "Genome annotation for clinical genomic diagnostics: strengths and weaknesses". Genome Medicine. 9 (1): 49. doi:10.1186/s13073-017-0441-1. ISSN 1756-994X. PMC 5448149. PMID 28558813.
- ↑ Harrow, J.; et al. (September 2012). "GENCODE: the reference human genome annotation for The ENCODE Project". Genome Res. 22 (9): 1760–74. doi:10.1101/gr.135350.111. PMC 3431492. PMID 22955987.
- ↑ Gibson G, Muse SV (2009). A primer of genome science (3rd ed.). Sunderland, MA: Sinauer Associates. ISBN 978-0-87893-236-8.
- ↑ "The human proteome in brain – The Human Protein Atlas". www.proteinatlas.org. Archived from the original on September 29, 2017. Retrieved September 29, 2017.
- ↑ Uhlén, Mathias; Fagerberg, Linn; Hallström, Björn M.; Lindskog, Cecilia; Oksvold, Per; Mardinoglu, Adil; Sivertsson, Åsa; Kampf, Caroline; Sjöstedt, Evelina (January 23, 2015). "Tissue-based map of the human proteome". Science. 347 (6220): 1260419. doi:10.1126/science.1260419. ISSN 0036-8075. PMID 25613900.
- ↑ Warden, A (2017). "Gene expression profiling in the human alcoholic brain". Neuropharmacology. 122: 161–174. doi:10.1016/j.neuropharm.2017.02.017. PMC 5479716. PMID 28254370.
- ↑ Farris, S.P.; et al. (2015). "Applying the new genomics to alcohol dependence". Alcohol. 49 (8): 825–36. doi:10.1016/j.alcohol.2015.03.001. PMC 4586299. PMID 25896098.
- ↑ Rozycka, A; Liguz-Lecznar, M (August 2017). "The space where aging acts: focus on the GABAergic synapse". Aging Cell. 16 (4): 634–643. doi:10.1111/acel.12605. PMC 5506442. PMID 28497576.
- ↑ Flores, CE; Méndez, P (2014). "Shaping inhibition: activity dependent structural plasticity of GABAergic synapses". Frontiers in Cellular Neuroscience. 8: 327. doi:10.3389/fncel.2014.00327. PMC 4209871. PMID 25386117.
- ↑ Miller, G. A. (March 1956). "The magical number seven plus or minus two: some limits on our capacity for processing information". Psychological Review. 63 (2): 81–97. ISSN 0033-295X. PMID 13310704.
- ↑ Pocock, G. ; Richards, C. (2006). Human Physiology: The Basis of Medicine (3rd ed.). Oxford: Oxford University Press. ISBN 978-0-19-856878-0. p 68.
- ↑ Flores A, Maldonado R, Berrendero F (December 2013). "Cannabinoid-hypocretin cross-talk in the central nervous system: what we know so far". Frontiers in Neuroscience. 7: 256. doi:10.3389/fnins.2013.00256. PMC 3868890. PMID 24391536. • Figure 1: Schematic of brain CB1 expression and orexinergic neurons expressing OX1 (HcrtR1) or OX2 (HcrtR2) • Figure 2: Synaptic signaling mechanisms in cannabinoid and orexin systems • Figure 3: Schematic of brain pathways involved in food intake
- ↑ Clark, B.D.; Goldberg, E.M.; Rudy, B. (December 2009). "Electrogenic tuning of the axon initial segment". The Neuroscientist. 15 (6): 651–68. doi:10.1177/1073858409341973. PMC 2951114. PMID 20007821.
- ↑ Freund TF, Katona I, Piomelli D (July 2003). "Role of endogenous cannabinoids in synaptic signaling". Physiological Reviews. 83 (3): 1017–66. doi:10.1152/physrev.00004.2003. PMID 12843414.
- ↑ Pocock, G. ; Richards, C. (2006). Human Physiology: The Basis of Medicine (3rd ed.). Oxford: Oxford University Press. ISBN 978-0-19-856878-0. p 70-74.
- ↑ "NIMH " Brain Basics". www.nimh.nih.gov. Archived from the original on March 26, 2017. Retrieved March 26, 2017.
- ↑ Purves, Dale (2011). Neuroscience (5. ed.). Sunderland, Mass.: Sinauer. p. 139. ISBN 978-0-87893-695-3.
- ↑ Melis M, Pistis M (December 2007). "Endocannabinoid signaling in midbrain dopamine neurons: more than physiology?". Current Neuropharmacology. 5 (4): 268–77. doi:10.2174/157015907782793612. PMC 2644494. PMID 19305743.
- ↑ Swaminathan, N (April 29, 2008). "Why Does the Brain Need So Much Power?". Scientific American. Archived from the original on January 27, 2014. Retrieved November 19, 2010.
- ↑ Wasserman DH (January 2009). "Four grams of glucose". American Journal of Physiology. Endocrinology and Metabolism. 296 (1): E11–21. doi:10.1152/ajpendo.90563.2008. PMC 2636990. PMID 18840763.
- ↑ Quistorff, B; Secher, N; Van Lieshout, J (July 24, 2008). "Lactate fuels the human brain during exercise". The FASEB Journal. 22 (10): 3443–3449. doi:10.1096/fj.08-106104. PMID 18653766. S2CID 15394163.
- ↑ Obel, L.F.; Müller, M.S.; Walls, A.B.; Sickmann, H.M.; Bak, L.K.; Waagepetersen, H.S.; Schousboe, A. (2012). "Brain glycogen-new perspectives on its metabolic function and regulation at the subcellular level". Frontiers in Neuroenergetics. 4: 3. doi:10.3389/fnene.2012.00003. PMC 3291878. PMID 22403540.
- ↑ Marin-Valencia, I.; et al. (February 2013). "Heptanoate as a neural fuel: energetic and neurotransmitter precursors in normal and glucose transporter I-deficient (G1D) brain". Journal of Cerebral Blood Flow and Metabolism. 33 (2): 175–82. doi:10.1038/jcbfm.2012.151. PMC 3564188. PMID 23072752.
- ↑ Tsuji, A. (2005). "Small molecular drug transfer across the blood-brain barrier via carrier-mediated transport systems". NeuroRx. 2 (1): 54–62. doi:10.1602/neurorx.2.1.54. PMC 539320. PMID 15717057.
- ↑ Vijay, N.; Morris, M.E. (2014). "Role of monocarboxylate transporters in drug delivery to the brain". Curr. Pharm. Des. 20 (10): 1487–98. doi:10.2174/13816128113199990462. PMC 4084603. PMID 23789956.
- ↑ Clark, D.D.; Sokoloff. L. (1999). Siegel, G.J.; Agranoff, B.W.; Albers, R.W.; Fisher, S.K.; Uhler, M.D. (eds.). Basic Neurochemistry: Molecular, Cellular and Medical Aspects. Philadelphia: Lippincott. pp. 637–670. ISBN 978-0-397-51820-3.
- ↑ Mrsulja, B.B. (2012). Pathophysiology of Cerebral Energy Metabolism. Springer Science & Business Media. pp. 2–3. ISBN 978-1-4684-3348-7.
- ↑ Raichle, M.; Gusnard, DA (2002). "Appraising the brain's energy budget". Proc. Natl. Acad. Sci. U.S.A. 99 (16): 10237–10239. Bibcode:2002PNAS...9910237R. doi:10.1073/pnas.172399499. PMC 124895. PMID 12149485.
- ↑ Gianaros, Peter J.; Gray, Marcus A.; Onyewuenyi, Ikechukwu; Critchley, Hugo D. (2010). "Chapter 50. Neuroimaging methods in behavioral medicine". In Steptoe, A. (ed.). Handbook of Behavioral Medicine: Methods and Applications. Springer Science & Business Media. p. 770. doi:10.1007/978-0-387-09488-5_50. ISBN 978-0-387-09488-5.
- ↑ Kuzawa, C. W.; Chugani, H. T.; Grossman, L. I.; Lipovich, L.; Muzik, O.; Hof, P. R.; Wildman, D. E.; Sherwood, C. C.; Leonard, W. R.; Lange, N. (2014-09-09). "Metabolic costs and evolutionary implications of human brain development". Proceedings of the National Academy of Sciences. 111 (36): 13010–13015. Bibcode:2014PNAS..11113010K. doi:10.1073/pnas.1323099111. ISSN 0027-8424. PMC 4246958. PMID 25157149.
- ↑ Bacyinski A, Xu M, Wang W, Hu J (November 2017). "The Paravascular Pathway for Brain Waste Clearance: Current Understanding, Significance and Controversy". Frontiers in Neuroanatomy. 11: 101. doi:10.3389/fnana.2017.00101. PMC 5681909. PMID 29163074.
- ↑ Xie L, Kang H, Xu Q, Chen MJ, Liao Y, Thiyagarajan M, O'Donnell J, Christensen DJ, Nicholson C, Iliff JJ, Takano T, Deane R, Nedergaard M (October 2013). "Sleep drives metabolite clearance from the adult brain". Science. 342 (6156): 373–377. Bibcode:2013Sci...342..373X. doi:10.1126/science.1241224. PMC 3880190. PMID 24136970.
- ↑ Tononi, Guilio; Cirelli, Chiara (August 2013). "Perchance to Prune" (PDF). Scientific American. 309 (2): 34–39. Bibcode:2013SciAm.309b..34T. doi:10.1038/scientificamerican0813-34. PMID 23923204. S2CID 54052089. Archived from the original (PDF) on 2018-12-26.
- ↑ "Brain Injury, Traumatic". Medcyclopaedia. GE. Archived from the original on May 26, 2011.
- ↑ Dawodu, S.T. (March 9, 2017). "Traumatic Brain Injury (TBI) – Definition and Pathophysiology: Overview, Epidemiology, Primary Injury". Archived from the original on April 9, 2017.
{{cite journal}}: Cite journal requires|journal=(help) - ↑ Davidson's 2010, pp. 1196–7.
- ↑ ۱۸۱٫۰ ۱۸۱٫۱ Davidson's 2010, pp. 1205–15.
- ↑ Davidson's 2010, pp. 1216–7.
- ↑ "NIMH " Brain Basics". www.nimh.nih.gov. Archived from the original on March 26, 2017. Retrieved March 26, 2017.
- ↑ Volkow, N.D.; Koob, G.F.; McLellan, A.T. (January 2016). "Neurobiologic advances from the brain disease model of addiction". The New England Journal of Medicine. 374 (4): 363–371. doi:10.1056/NEJMra1511480. PMC 6135257. PMID 26816013.
- ↑ "Status Epilepticus". Epilepsy Foundation.
- ↑ Davidson's 2010, pp. 1172–9.
- ↑ Pennington, B.F. (2008). Diagnosing Learning Disorders, Second Edition: A Neuropsychological Framework. Guilford Press.
- ↑ Perese, E.F. (2012). Psychiatric Advanced Practice Nursing: A Biopsychsocial Foundation for Practice. F.A. Davis. pp. 82–88.
- ↑ Harbison, J.; Massey, A.; Barnett, L.; Hodge, D.; Ford, G.A. (June 1999). "Rapid ambulance protocol for acute stroke". Lancet. 353 (9168): 1935. doi:10.1016/S0140-6736(99)00966-6. PMID 10371574.
- ↑ Davidson's 2010, p. 1183.
- ↑ Davidson's 2010, pp. 1180–1.
- ↑ Davidson's 2010, pp. 1181, 1183–1185.
- ↑ ۱۹۳٫۰ ۱۹۳٫۱ ۱۹۳٫۲ Davidson's 2010, pp. 1183–1185.
- ↑ Davidson's 2010, pp. 1185-1189.
- ↑ Goyal, M.; et al. (April 2016). "Endovascular thrombectomy after large-vessel ischaemic stroke: a meta-analysis of individual patient data from five randomised trials". The Lancet. 387 (10029): 1723–1731. doi:10.1016/S0140-6736(16)00163-X. PMID 26898852.
- ↑ Saver, J. L. (December 8, 2005). "Time is brain—quantified". Stroke. 37 (1): 263–266. doi:10.1161/01.STR.0000196957.55928.ab. PMID 16339467.
- ↑ Davidson's 2010, pp. 1185–1189.
- ↑ Winstein, C.J.; et al. (June 2016). "Guidelines for adult stroke rehabilitation and recovery". Stroke. 47 (6): e98–e169. doi:10.1161/STR.0000000000000098. PMID 27145936.
- ↑ Kuźma, Elżbieta; Lourida, Ilianna; Moore, Sarah F.; Levine, Deborah A.; Ukoumunne, Obioha C.; Llewellyn, David J. (November 2018). "Stroke and dementia risk: A systematic review and meta-analysis". Alzheimer's & Dementia. 14 (11): 1416–1426. doi:10.1016/j.jalz.2018.06.3061. ISSN 1552-5260. PMC 6231970. PMID 30177276.
- ↑ ۲۰۰٫۰ ۲۰۰٫۱ ۲۰۰٫۲ Goila, AK; Pawar, M (2009). "The diagnosis of brain death". Indian Journal of Critical Care Medicine. 13 (1): 7–11. doi:10.4103/0972-5229.53108. PMC 2772257. PMID 19881172.
- ↑ ۲۰۱٫۰ ۲۰۱٫۱ ۲۰۱٫۲ Wijdicks, EFM (January 8, 2002). "Brain death worldwide: accepted fact but no global consensus in diagnostic criteria". Neurology. 58 (1): 20–25. doi:10.1212/wnl.58.1.20. PMID 11781400.
- ↑ Dhanwate, AD (September 2014). "Brainstem death: A comprehensive review in Indian perspective". Indian Journal of Critical Care Medicine. 18 (9): 596–605. doi:10.4103/0972-5229.140151. PMC 4166875. PMID 25249744.
- ↑ Davidson's 2010, p. 200.
- ↑ ۲۰۴٫۰ ۲۰۴٫۱ Davidson's 2010.
- ↑ Pawar, Mridula; Goila, Ajay Kumar (March 2009). "The diagnosis of brain death". Indian Journal of Critical Care Medicine (به انگلیسی). 13 (1): 7–11. doi:10.4103/0972-5229.53108. ISSN 0972-5229. PMC 2772257. PMID 19881172.
{{cite journal}}: نگهداری یادکرد:فرمت پارامتر PMC (link) - ↑ Kandel, ER; Schwartz JH; Jessell TM (2000). Principles of Neural Science (4th ed.). New York: McGraw-Hill. ISBN 978-0-8385-7701-1.
- ↑ ۲۰۷٫۰ ۲۰۷٫۱ Gross, Charles G. (1987). Adelman, George (ed.). Encyclopedia of neuroscience (PDF) (2. ed.). Boston: Birkhäeuser. pp. 843–847. ISBN 978-0-8176-3335-6. Archived (PDF) from the original on May 5, 2013.
- ↑ Bear, M.F.; B.W. Connors; M.A. Paradiso (2001). Neuroscience: Exploring the Brain. Baltimore: Lippincott. ISBN 978-0-7817-3944-3.
- ↑ von Staden, p.157
- ↑ ۲۱۰٫۰ ۲۱۰٫۱ Gross, Charles G. (1987). Adelman, George (ed.). Encyclopedia of neuroscience (PDF) (2. ed.). Boston: Birkhäeuser. pp. 843–847. ISBN 978-0-8176-3335-6. Archived (PDF) from the original on May 5, 2013.
- ↑ Bear, M.F.; B.W. Connors; M.A. Paradiso (2001). Neuroscience: Exploring the Brain. Baltimore: Lippincott. ISBN 978-0-7817-3944-3.
- ↑ Swanson, Larry W. (August 12, 2014). Neuroanatomical Terminology: A Lexicon of Classical Origins and Historical Foundations. Oxford University Press. ISBN 978-0-19-534062-4.
- ↑ ۲۱۳٫۰ ۲۱۳٫۱ Lokhorst, Gert-Jan (January 1, 2016). "Descartes and the Pineal Gland". The Stanford Encyclopedia of Philosophy. Metaphysics Research Lab, Stanford University. Retrieved March 11, 2017.
- ↑ ۲۱۴٫۰ ۲۱۴٫۱ ۲۱۴٫۲ ۲۱۴٫۳ ۲۱۴٫۴ Gross, Charles G. (1999). Brain, vision, memory: tales in the history of neuroscience (1st MIT Press pbk. ed.). Cambridge, Mass.: MIT. pp. 37–51. ISBN 978-0-262-57135-7.
- ↑ Marshall, Louise H.; Magoun, Horace W. (March 9, 2013). Discoveries in the Human Brain: Neuroscience Prehistory, Brain Structure, and Function. Springer Science & Business Media. p. 44. ISBN 978-1-4757-4997-7.
- ↑ Holtz, Anders; Levi, Richard (July 20, 2010). Spinal Cord Injury. Oxford University Press. ISBN 978-0-19-970681-5.
- ↑ Tessman, Patrick A.; Suarez, Jose I. (December 2020). "Influence of early printmaking on the development of neuroanatomy and neurology". Archives of Neurology. 59 (12): 1964–1969. doi:10.1001/archneur.59.12.1964. ISSN 0003-9942. PMID 12470188.
- ↑ O'Connor, James P. B. (March 2003). "Thomas Willis and the background to Cerebri Anatome". Journal of the Royal Society of Medicine. 96 (3): 139–143. doi:10.1258/jrsm.96.3.139. ISSN 0141-0768. PMID 12612118.
- ↑ EMERY, ALAN (October 2000). "A Short History of Neurology: The British Contribution 1660–1910". Journal of Anatomy. 197 (Pt 3): 513–518. doi:10.1046/j.1469-7580.2000.197305131.x. ISSN 0021-8782. PMC 1468164.
- ↑ Sabbatini, Renato M.E. "Sabbatini, R.M.E. : The Discovery of Bioelectricity. Nerve Conduction". www.cerebromente.org.br. Archived from the original on June 26, 2017. Retrieved June 10, 2017.
- ↑ Karbowski, K. (1990). "Sixty years of clinical electroencephalography". European Neurology. 30 (3): 170–175. doi:10.1159/000117338. ISSN 0014-3022. PMID 2192889.
- ↑ Pearce, J. M. S. (March 17, 2009). "Marie-Jean-Pierre Flourens (1794-1867) and cortical localization". European Neurology. 61 (5): 311–314. doi:10.1159/000206858. ISSN 1421-9913. PMID 19295220.
- ↑ ۲۲۳٫۰ ۲۲۳٫۱ ۲۲۳٫۲ De Carlos, Juan A.; Borrell, José (August 2007). "A historical reflection of the contributions of Cajal and Golgi to the foundations of neuroscience". Brain Research Reviews. 55 (1): 8–16. doi:10.1016/j.brainresrev.2007.03.010. ISSN 0165-0173. PMID 17490748.
- ↑ Burke, Robert E. (April 2007). "Sir Charles Sherrington's the integrative action of the nervous system: a centenary appreciation". Brain: A Journal of Neurology. 130 (Pt 4): 887–894. doi:10.1093/brain/awm022. ISSN 1460-2156. PMID 17438014.
- ↑ Squire, Larry R., ed. (1996). The history of neuroscience in autobiography. Washington DC: Society for Neuroscience. pp. 475–97. ISBN 978-0-12-660305-7.
- ↑ Cowan, W. M.; Harter, D. H.; Kandel, E. R. (2000). "The emergence of modern neuroscience: some implications for neurology and psychiatry". Annual Review of Neuroscience. 23: 343–391. doi:10.1146/annurev.neuro.23.1.343. ISSN 0147-006X. PMID 10845068.
- ↑ Brady, Joseph V.; Nauta, Walle J. H. (October 22, 2013). Principles, Practices, and Positions in Neuropsychiatric Research: Proceedings of a Conference Held in June 1970 at the Walter Reed Army Institute of Research, Washington, D.C. , in Tribute to Dr. David Mckenzie Rioch upon His Retirement as Director of the Neuropsychiatry Division of That Institute. Elsevier. p. vii. ISBN 978-1-4831-5453-4.
- ↑ Adelman, George (2010-01-15). "The neurosciences research program at MIT and the beginning of the modern field of neuroscience". Journal of the History of the Neurosciences. 19 (1): 15–23. doi:10.1080/09647040902720651. ISSN 1744-5213. PMID 20391098.
- ↑ ۲۲۹٫۰ ۲۲۹٫۱ Principles of Neural Science, 4th ed. Eric R. Kandel, James H. Schwartz, Thomas M. Jessel, eds. McGraw-Hill:New York, NY. 2000.
- ↑ Papez, J. W. (February 1995). "A proposed mechanism of emotion. 1937". The Journal of Neuropsychiatry and Clinical Neurosciences. 7 (1): 103–112. doi:10.1176/jnp.7.1.103. ISSN 0895-0172. PMID 7711480.
- ↑ Lambert, Kelly G. (August 2003). "The life and career of Paul MacLean. a journey toward neurobiological and social harmony". Physiology & Behavior. 79 (3): 343–349. doi:10.1016/s0031-9384(03)00147-1. ISSN 0031-9384. PMID 12954429.
- ↑ Chatterjee, Anjan; Coslett, H. Branch (December 2013). The Roots of Cognitive Neuroscience: Behavioral Neurology and Neuropsychology. OUP USA. pp. 337–8. ISBN 978-0-19-539554-9.
- ↑ Bliss, Michael (October 1, 2005). Harvey Cushing: A Life in Surgery: A Life in Surgery. USA: Oxford University Press. pp. ix–x. ISBN 978-0-19-534695-4.
- ↑ Kretzer, Ryan M.; Coon, Alexander L.; Tamargo, Rafael J. (June 2010). "Walter E. Dandy's contributions to vascular neurosurgery". Journal of Neurosurgery. 112 (6): 1182–1191. doi:10.3171/2009.7.JNS09737. ISSN 1933-0693. PMID 20515365.
- ↑ Domínguez D, Juan F.; Lewis, E. Douglas; Turner, Robert; Egan, Gary F. (2009). "The brain in culture and culture in the brain: a review of core issues in neuroanthropology". Progress in Brain Research. 178: 43–64. doi:10.1016/S0079-6123(09)17804-4. ISSN 1875-7855. PMID 19874961.
- ↑ "Cultural Environment Influences Brain Function | Psych Central News". Psych Central News. August 4, 2010. Archived from the original on January 17, 2017.
- ↑ ۲۳۷٫۰ ۲۳۷٫۱ Macmillan, Malcolm B. (2000). An Odd Kind of Fame: Stories of Phineas Gage. MIT Press. ISBN 978-0-262-13363-0.
- ↑ Rescher, N. (1992). G. W. Leibniz's Monadology. Psychology Press. p. 83. ISBN 978-0-415-07284-7.
- ↑ Hart, WD (1996). Guttenplan S (ed.). A Companion to the Philosophy of Mind. Blackwell. pp. 265–267.
- ↑ Churchland, P.S. (1989). "Ch. 8". Neurophilosophy. MIT Press. ISBN 978-0-262-53085-9.
- ↑ Selimbeyoglu, Aslihan; Parvizi, J (2010). "Electrical stimulation of the human brain: perceptual and behavioral phenomena reported in the old and new literature". Frontiers in Human Neuroscience. 4: 46. doi:10.3389/fnhum.2010.00046. PMC 2889679. PMID 20577584.
- ↑ Macmillan, Malcolm B. (2000). An Odd Kind of Fame: Stories of Phineas Gage. MIT Press. ISBN 978-0-262-13363-0.
- ↑ Lilienfeld, S.O.; Lynn, S.J.; Ruscio, J.; Beyerstein, B.L. (2011). 50 Great Myths of Popular Psychology: Shattering Widespread Misconceptions about Human Behavior. John Wiley & Sons. p. 89. ISBN 978-1-4443-6074-5.
- ↑ McDaniel, M. (2005). "Big-brained people are smarter" (PDF). Intelligence. 33 (4): 337–346. doi:10.1016/j.intell.2004.11.005. Archived (PDF) from the original on September 6, 2014.
- ↑ Luders, E.; et al. (September 2008). "Mapping the relationship between cortical convolution and intelligence: effects of gender". Cerebral Cortex. 18 (9): 2019–26. doi:10.1093/cercor/bhm227. PMC 2517107. PMID 18089578.
- ↑ Hoppe, C; Stojanovic, J (2008). "High-Aptitude Minds". Scientific American Mind. 19 (4): 60–67. doi:10.1038/scientificamericanmind0808-60.
- ↑ "Tupaia belangeri". The Genome Institute, Washington University. Archived from the original on June 1, 2010. Retrieved January 22, 2016.
- ↑ Carrier, Martin; Mittelstrass, Jürgen (1991). Mind, Brain, Behavior: The Mind-body Problem and the Philosophy of Psychology [Geist, Gehirn, Verhalten]. Translated by Lindberg, Steven (revised and expanded English ed.). Berlin: Walter de Gruyter. p. 11. ISBN 978-3-11-012876-5. Retrieved 22 May 2021.
- ↑ Cobb, Matthew (April 21, 2020). The Idea of the Brain: The Past and Future of Neuroscience. New York: Hachette UK (published 2020). ISBN 978-1-5416-4686-5. Retrieved 22 May 2021.
- ↑ Jarrett, C. (November 17, 2014). Great Myths of the Brain. John Wiley & Sons. ISBN 978-1-118-31271-1.
- ↑ Phillips, Helen (July 11, 2002). "Video game "brain damage" claim criticised". New Scientist. Archived from the original on January 11, 2009. Retrieved February 6, 2008.
- ↑ Popova, Maria (August 18, 2011). "'Brain Culture': How Neuroscience Became a Pop Culture Fixation". The Atlantic. Archived from the original on July 28, 2017.
- ↑ Thornton, Davi Johnson (2011). Brain Culture. Neuroscience and Popular Media. Rutgers University Press. ISBN 978-0-8135-5013-8.
- ↑ Cyborgs and Space بایگانیشده در اکتبر ۶, ۲۰۱۱ توسط Wayback Machine, in Astronautics (September 1960), by Manfred E. Clynes and Nathan S. Kline.
- ↑ Bergfelder, Tim (2005). International Adventures: German Popular Cinema and European Co-productions in the 1960s. Berghahn Books. p. 129. ISBN 978-1-57181-538-5.
- ↑ Glees, Paul (2005). The Human Brain. Cambridge University Press. p. 1. ISBN 978-0-521-01781-7.
- ↑ Bornstein, Marc H.; Lamb, Michael E. (2015). Developmental Science: An Advanced Textbook. Psychology Press. p. 220. ISBN 978-1-136-28220-1.
- ↑ ۲۵۸٫۰ ۲۵۸٫۱ Bernstein, Douglas (2010). Essentials of Psychology. Cengage Learning. p. 64. ISBN 978-0-495-90693-3.
- ↑ Simpkins, C. Alexander; Simpkins, Annellen M. (2012). Neuroscience for Clinicians: Evidence, Models, and Practice. Springer Science & Business Media. p. 143. ISBN 978-1-4614-4842-6.
- ↑ Hofman, Michel A. (March 27, 2014). "Evolution of the human brain: when bigger is better". Frontiers in Neuroanatomy. 8: 15. doi:10.3389/fnana.2014.00015. PMC 3973910. PMID 24723857.
- ↑ Gray, Peter (2002). Psychology (4th ed.). Worth Publishers. ISBN 978-0-7167-5162-5. OCLC 46640860.
- ↑ Lu, Zhong-Lin; Dosher, Barbara (2013). Visual Psychophysics: From Laboratory to Theory. MIT Press. p. 3. ISBN 978-0-262-01945-3.
- ↑ Sharwood Smith, Mike (2017). Introducing Language and Cognition. Cambridge University Press. p. 206. ISBN 978-1-107-15289-2.
- ↑ Nieuwenhuys, Rudolf; ten Donkelaar, Hans J.; Nicholson, Charles (2014). The Central Nervous System of Vertebrates. Springer. p. 2127. ISBN 978-3-642-18262-4.
- ↑ Kolb, Bryan; Whishaw, Ian Q. (2013). Introduction to Brain and Behavior. Macmillan Higher Education. p. 21. ISBN 978-1-4641-3960-4.
- ↑ Lerner, Lee; Lerner, Brenda Wilmoth (2004). The Gale Encyclopedia of Science: Pheasants-Star. Gale. p. 3759. ISBN 978-0-7876-7559-2.
As human's position changed and the manner in which the skull balanced on the spinal column pivoted, the brain expanded, altering the shape of the cranium.
- ↑ Begun, David R. (2012). A Companion to Paleoanthropology. John Wiley & Sons. p. 388. ISBN 978-1-118-33237-5.
- ↑ Jones, R. (2012). "Neurogenetics: What makes a human brain?". Nature Reviews Neuroscience. 13 (10): 655. doi:10.1038/nrn3355. PMID 22992645. S2CID 44421363.
- ↑ Gray's Anatomy 2008, p. 275.
- ↑ Davidson's 2010, p. 1158.
کتابشناسی ویرایش
- Colledge, Nicki R.; Walker, Brian R.; Ralston, Stuart H.; Ralston, eds. (2010). Davidson's Principles and Practice of Medicine (21st ed.). Edinburgh: Churchill Livingstone/Elsevier. ISBN 978-0-7020-3085-7.
- Hall, John (2011). Guyton and Hall Textbook of Medical Physiology (12th ed.). Philadelphia, PA: Saunders/Elsevier. ISBN 978-1-4160-4574-8.
- Larsen, William J. (2001). Human Embryology (3rd ed.). Philadelphia, PA: Churchill Livingstone. ISBN 978-0-443-06583-5.
- Bogart, Bruce Ian; Ort, Victoria (2007). Elsevier's Integrated Anatomy and Embryology. Philadelphia, PA: Elsevier Saunders. ISBN 978-1-4160-3165-9.
- Pocock, G.; Richards, C. (2006). Human Physiology: The Basis of Medicine (3rd ed.). Oxford: Oxford University Press. ISBN 978-0-19-856878-0.
- Purves, Dale (2012). Neuroscience (5th ed.). Sunderland, MA: Sinauer associates. ISBN 978-0-87893-695-3.
- Squire, Larry (2013). Fundamental Neuroscience. Waltham, MA: Elsevier. ISBN 978-0-12-385870-2.
- Standring, Susan, ed. (2008). Gray's Anatomy: The Anatomical Basis of Clinical Practice (40th ed.). London: Churchill Livingstone. ISBN 978-0-8089-2371-8.
پیوند به بیرون ویرایش
- «آمار و ارقام مغز». دانشگاه واشینگتن. دریافتشده در ۲۰۲۲-۰۲-۱۳. (انگلیسی)
- «آناتومی مغز و نحوه عملکرد مغز». دانشگاه جانز هاپکینز. دریافتشده در ۲۰۲۲-۰۲-۱۳. (انگلیسی)
- Hoffman، Matthew؛ MD. «مغز (آناتومی انسان): تصویر، عملکرد، قطعات، شرایط و موارد دیگر». WebMD. دریافتشده در ۲۰۲۲-۰۲-۱۳. (انگلیسی)
- «مغز | تعریف، بخشها، توابع، و حقایق». بریتانیکا. دریافتشده در ۲۰۲۲-۰۲-۱۳. (انگلیسی)
- «صفحه پروژه مغز انسان». پروژه مغز. دریافتشده در ۲۰۲۲-۰۲-۱۳. (انگلیسی)
- «مبانی مغز: مغز خود را بشناسید». مؤسسه ملی اختلالات عصبی و سکته مغزی. دریافتشده در ۲۰۲۲-۰۲-۱۳. (انگلیسی)
- «مغز انسان: اطلاعات، حقایق و اخبار به همراه ویدئو». نشنال جئوگرافی. ۲۰۰۹-۱۰-۱۵. دریافتشده در ۲۰۲۲-۰۲-۱۳. (انگلیسی)